Алкены – это органические соединения, которые содержат двойную связь между углеродными атомами. Благодаря этой необычной структуре алкены обладают рядом особенностей, одной из которых является их низкая реактивность по сравнению с другими классами органических соединений. Вот почему алкены не реагируют с водой, галогенами и металлами.
Начнем с реакции алкенов с водой. Хотя алкены имеют двойную связь, которая обычно является реакционноспособной, они не реагируют со водой. Это происходит потому, что углеродные атомы, связанные двойной связью, уже насыщены водородом и не обладают свободными электронами, необходимыми для образования новых химических связей. Таким образом, алкены не могут быть обратимо гидратированы в присутствии воды.
Следующая группа веществ, с которыми алкены не реагируют, - это галогены. Галогены, такие как хлор, бром и йод, обычно обладают высокой реакционной способностью. Однако, из-за своей специфической химической структуры, алкены не реагируют с галогенами. Происходит это потому, что галогены образуют слабые связи с углеродом, и двойная связь в алкене недостаточно реакционноспособна, чтобы конкурировать с реакцией галогена со водородом или другими атомами углеводорода.
Металлы также не реагируют с алкенами. Хотя многие металлы обычно обладают высокой реакционной способностью, алкены не образуют с ними химические связи. Это обусловлено тем, что двойная связь в алкене имеет высокую энергию, и ее деформация для образования связи с металлом является неточной.
Таким образом, из-за своей специфической химической структуры алкены не реагируют с водой, галогенами и металлами. Эти особенности делают их полезными во множестве органических синтезов и промышленных процессов, где требуется сохранение двойной связи.
Алкены и их неактивность
Алкены - это органические соединения, содержащие двойные связи между атомами углерода. Одно из основных свойств алкенов - их неактивность по отношению к воде, галогенам и металлам.
Неактивность алкенов в отношении воды обусловлена силой связи между атомами углерода. Двойная связь состоит из сигма-связи, образованной перекрывающимися p-орбиталями, и пи-связи, образованной неперекрывающимися p-орбиталями. Пи-связь является относительно слабой и неустойчивой, что приводит к тому, что алкены не растворяются в воде и не реагируют с ней.
Также, алкены не реагируют с галогенами, такими как хлор, бром и йод. Это объясняется тем, что галогены - это высокоэнергетические вещества, которые могут реагировать с ненасыщенными соединениями, такими как алкены. Однако, из-за сильной связи в пи-связи, алкены не обладают достаточной энергией для активной реакции с галогенами.
Алкены также не реагируют с металлами. Это связано с тем, что металлы имеют высокую электроотрицательность и могут образовывать ионные связи. Алкены не содержат отрицательно заряженных атомов и не могут образовывать стабильные ионные связи с металлами.
Таким образом, неактивность алкенов по отношению к воде, галогенам и металлам обусловлена силой пи-связи между атомами углерода, что делает их устойчивыми и неспособными к активным реакциям с этими веществами.
Почему алкены не реагируют с водой?
Алкены – это класс органических соединений, характеризующихся наличием двойной связи между углеродными атомами. В отличие от алканов, которые содержат только однонепрерывные углеводородные цепи, алкены обладают высокой химической активностью, но не реагируют с водой в нормальных условиях.
Двойная связь в молекуле алкена представляет собой особую структуру, которая обладает высокой энергией и требует существенной активации для расщепления. Вода является пассивным агентом в реакциях с алкенами, и ее молекулы не обладают достаточной активностью, чтобы позволить проходу реакции.
Также стоит отметить, что вода обладает полярной структурой, в то время как алкены являются неполярными соединениями. Это различие в полярности не позволяет молекулам алкена и воды образовать стабильную химическую связь.
Однако, с высокой активацией и присутствием специальных катализаторов, алкены все же могут реагировать с водой. Например, в присутствии кислорода и высоких температур происходит окислительное разложение алкенов, которое сопровождается реакцией с водой.
Итак, в нормальных условиях алкены не реагируют с водой из-за высокой энергии двойной связи, низкой активности воды и различия в их полярности. Однако, с использованием специальных условий, возможно разложение алкенов с участием воды.
Почему алкены не реагируют с галогенами?

Алкены - это органические соединения, содержащие двойную связь между атомами углерода. Галогены - это элементы группы 17 периодической системы, такие как хлор, бром, йод и фтор, которые обладают высокой электроотрицательностью.
Причина, по которой алкены не реагируют с галогенами, заключается в отсутствии достаточной полярности в двойной связи. Электроотрицательные галогены имеют сильную тягу к электронам и обычно реагируют с атомами углерода, имеющими положительные частичные заряды.
Однако в случае алкенов, электроотрицательность галогенов не приводит к образованию достаточно сильного положительного заряда на атоме углерода. Это связано с тем, что электронная плотность в двойной связи алкена распределена равномерно между двумя атомами углерода и не создает полярности как в случае одиночной связи.
Таким образом, отсутствие достаточной полярности в алкенах препятствует реакции с галогенами, которые требуют положительных зарядов на атомах углерода для реакции обмена.
Почему алкены не реагируют с металлами?
Алкены - это органические соединения, в которых углеродные атомы образуют двойные связи. В отличие от алканов, которые содержат только одиночные связи, алкены обладают более высокой степенью ненасыщенности.
Не смотря на свою ненасыщенность, алкены не образуют прямой реакции с металлами. Это объясняется высокой прочностью и устойчивостью связи между углеродным и водородным атомами.
Во-первых, связь С-С в алкенах является двойной связью, состоящей из одной сигма-связи и одной пи-связи. Пи-связь представляет собой слабую связь с высокой энергией и требует большого количества энергии для ее разрыва. Металлы обычно не обладают такой энергией, чтобы разорвать пи-связь и образовать новую связь с атомом углерода.
Во-вторых, алкены обладают высокой степенью стабильности благодаря электронной конфигурации двойной связи. При образовании связи между металлом и атомом углерода электроны будут потеряны или переданы от металла к углероду, что противоречит энергетической структуре алкена и создает энергетическое барьер для реакции.
Таким образом, из-за прочности связи С-С и электронной структуры алкена, металлы не взаимодействуют с алкенами напрямую. Однако, существуют специфические реакции, в которых алкены могут вступать с металлами, но они требуют особых условий или использования катализаторов.
Неактивность алкенов и их структура
Алкены - органические соединения, которые состоят из углеродных атомов, связанных двойными связями. Они представляют собой насыщенные углеводороды и обладают такими особенностями, как низкая активность и относительная стабильность. Неактивность алкенов объясняется их структурой и особыми химическими свойствами.
Одной из причин неактивности алкенов является наличие двойной связи между углеродными атомами. Двойная связь обладает высокой жесткостью и не позволяет молекуле алкена иметь свободное вращение вокруг связи. Это препятствует свободному доступу других веществ к двойной связи и затрудняет реакции с водой, галогенами и металлами.
Помимо этого, электродонорные свойства алкенов играют роль в их неактивности. В двойной связи углеродного атома электроны сосредоточены между двумя атомами углерода. Это делает двойную связь не полностью поляризованной, что препятствует образованию различных химических связей и реакций с другими веществами.
Кроме того, сопряженность в молекуле алкена также влияет на его неактивность. Сопряженность, связанная с наличием пи-электронных облаков, делает алкены электронно более плотными и стабильными. Это препятствует реакциям с водой, галогенами и металлами, которые требуют активных электронных атомов для образования новых связей.
Таким образом, неактивность алкенов обусловлена их структурой, в особенности двойной связью, электродонорными свойствами и сопряженностью молекулы. Эти особенности препятствуют химическим реакциям алкенов с водой, галогенами и металлами, делая их стабильными и слабо реакционноспособными соединениями.
Почему алкены имеют меньшую активность, чем алканы?
1. Связь в алкенах является π-связью
Основное отличие алкенов от алканов состоит в типе связи между атомами углерода. В отличие от алканов, связь в алкенах представляет собой π-связь, которая более слабая по сравнению с σ-связью, присутствующей в алканах. Из-за этого алкены обладают меньшей активностью в химических реакциях.
2. Наличие двойной связи
В качестве π-связи алкена присутствует двойная связь между атомами углерода. Эта двойная связь блокирует доступ реагентов к углеродным атомам, снижая активность алкенов в химических реакциях. В то же время, в алканах отсутствует двойная связь, что обеспечивает большую активность соединений.
3. Стабилизация π-связи в алкенах
Алкены обладают возможностью стабилизировать π-связь благодаря наличию сопряженных пи-электронных облаков, которые создают эффект конъюгации. Это означает, что пи-электроны в алкенах могут перемещаться по цепочке углеродных атомов, что обеспечивает дополнительную стабильность молекулы. В результате, π-связь в алкенах становится менее активной и менее подвержена химическим реакциям.
4. Низкая полярность π-связи
Полярность связи в алкенах также влияет на их активность в химических реакциях. По сравнению с σ-связью, π-связь в алкенах является менее полярной, что делает молекулу алкена менее активной в реакциях с другими веществами, включая воду, галогены и металлы.
5. Сниженная реакционная способность
В результате всех перечисленных факторов, алкены обладают сниженной реакционной способностью по сравнению с алканами. Это означает, что алкены реагируют медленнее или вообще не реагируют с некоторыми химическими реагентами, такими как вода, галогены и металлы.
Причины неактивности алкенов
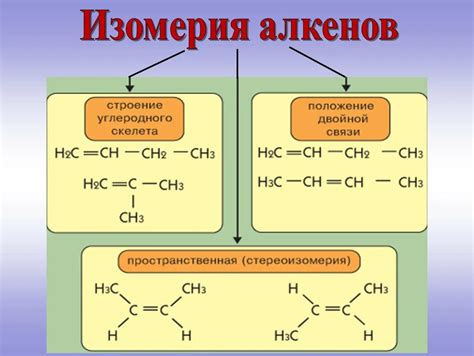
Неактивность алкенов - это особенность их реакционной способности, которая определяется их молекулярной структурой. Существует несколько причин, почему алкены не проявляют активность в реакциях с водой, галогенами и металлами.
- Недостаток полярности: алкены состоят из углеродных и водородных атомов, что делает их молекулы неполярными или слабо полярными. Вода, галогены и металлы обладают полярными или ионными связями, что требует наличия заряженных частиц для реакции. В связи с этим, алкены не могут реагировать с этими веществами.
- Стабильность двойной связи: в молекулах алкенов присутствует двойная углерод-углеродная связь, которая является более сильной и стабильной, чем одинарная связь. Это обусловлено сопряженностью пи-электронов, которая способствует укреплению связи. Благодаря этой стабильности, алкены не с легкостью реагируют с реагентами, такими как вода, галогены и металлы.
- Отсутствие электрофильных центров: в молекулах алкенов электрофильные центры, способные привлекать электроны в химической реакции, расположены вблизи двойной связи. Это снижает эффективность реагирования с нуклеофилами, такими как вода, галогены и металлы. В связи с этим, алкены могут быть менее активными в сравнении с другими органическими соединениями.
В целом, неактивность алкенов в реакциях с водой, галогенами и металлами объясняется их молекулярной структурой, особенностями связей и отсутствием электрофильных центров. Это делает их менее подходящими для многих реакций, которые характерны для других органических соединений.
Вопрос-ответ
Почему алкены не реагируют с водой?
Алкены не реагируют с водой из-за отсутствия полярного связывания между этими двумя веществами. Вода является полярным соединением, а алкены - неполярными. Из-за различия в полярности, они не взаимодействуют между собой.
Почему алкены не реагируют с галогенами?
Алкены не реагируют с галогенами из-за их структурной особенности. У молекул галогенов (например, хлора или брома) есть двойная связь, а у алкенов есть также двойная связь. Обе молекулы насыщены электронами, следовательно, не происходит электронного перераспределения и реакция не происходит.
Почему алкены не реагируют с металлами?
Алкены не реагируют с металлами из-за более высокой энергии связи между атомами углерода в алкене по сравнению с энергией связи между металлом и атомом углерода. Молекулы алкенов обладают более сильными электронными облаками, что делает их более стабильными и малоактивными в реакциях с металлами.
Почему алкены не реагируют с водой, галогенами и металлами?
Алкены не реагируют с водой, галогенами и металлами из-за структурных особенностей этих соединений и их низкой реакционной активности. Вода, галогены и металлы имеют специфические свойства и энергетические параметры, которые не позволяют им взаимодействовать с алкенами.
Почему неполярные алкены не могут реагировать с полярными веществами, такими как вода?
Неполярные алкены не могут реагировать с полярными веществами, такими как вода, из-за различия в полярности между этими веществами. Вода является полярным соединением с частично заряженными молекулами, в то время как алкены - неполярные соединения с равномерно распределенными электронами. Из-за этого различия нет электронного перетаскивания, что не позволяет им реагировать друг с другом.
