Металлы являются одной из основных групп химических элементов. Они обладают рядом характеристических свойств, отличающих их от других классов элементов, таких как неметаллы и полуметаллы. Металлы обычно обладают высокой электропроводностью, металлическим блеском, высокой пластичностью и деформируемостью, а также хорошей теплоотдачей.
Химические свойства металлов также отличаются от других элементов. Металлы имеют тенденцию образовывать положительные ионы, теряя один или несколько электронов. Это связано с низкой энергией их внешнего электронного оболочки и большими размерами атома. Более того, металлы обладают способностью реагировать с кислородом, образуя оксиды, и с водой, образуя гидроксиды.
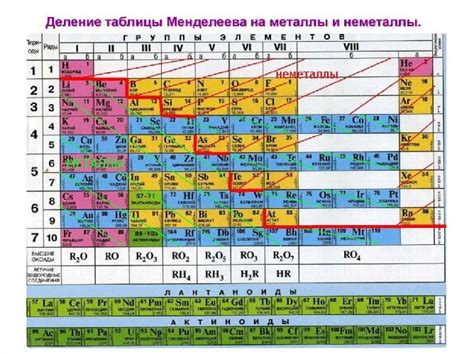
Таблица периодических закономерностей предоставляет систематическую информацию о различных свойствах металлов. Например, металлы располагаются слева от линии, проходящей поставиями полуметаллами и неметаллами, в таблице Менделеева. Они также имеют низкую электроотрицательность и высокую плотность. В зависимости от своего положения в таблице, металлы могут обладать различными свойствами, например, быть тяжелыми и прочными (такие, как железо), или быть более реактивными и легкими (такие, как литий).
Свойства металлов

1. Проводимость электричества и тепла: Металлы обладают высокой проводимостью электричества и тепла. Это связано со свободным движением электронов в их структуре. Именно благодаря этому свойству металлы широко используются в производстве проводников и теплообменных устройств.
2. Металлический блеск: Металлы обладают своеобразным металлическим блеском, который проявляется благодаря их способности отражать свет. Это делает металлы привлекательными для использования в ювелирных изделиях и декоративных элементах.
3. Пластичность и деформируемость: Металлы обладают высокой пластичностью, то есть их можно легко деформировать без разрушения структуры. Благодаря этому свойству металлы широко используются в производстве различных изделий, от автомобилей до посуды.
4. Прочность: Металлы являются прочными материалами с высокой степенью механической прочности. Это означает, что они способны выдерживать большие нагрузки без разрушения. Прочность металлов делает их незаменимыми в строительстве, машиностроении и других отраслях промышленности.
5. Способность образовывать сплавы: Металлы могут образовывать сплавы, то есть смеси с другими металлами или неметаллическими элементами. Это позволяет создавать материалы с новыми свойствами, например, повышенной прочностью или коррозионной стойкостью.
6. Коррозионная стойкость: Некоторые металлы обладают высокой коррозионной стойкостью, что означает, что они не подвержены разрушению при контакте с агрессивными средами, такими как кислоты или соли. Это делает эти металлы незаменимыми для изготовления емкостей и трубопроводов, используемых в химической и нефтегазовой промышленности.
7. Высокая плотность: Металлы обладают высокой плотностью, то есть большой массой в единицу объема. Это свойство делает металлы тяжелыми и прочными материалами, которые подходят для использования в качестве конструкционных элементов.
8. Высокая температура плавления: Большинство металлов обладает высокой температурой плавления, что означает, что они могут быть переведены в жидкое состояние при очень высоких температурах. Это позволяет использовать металлы в процессах плавления и литья для создания сложных форм и изделий.
Химические свойства металлов
Металлы – это особый класс веществ, который характеризуется не только физическими свойствами, но и химическими реакциями, протекающими на их поверхности. Химические свойства металлов определяются их электрохимической активностью и способностью образовывать соединения с другими элементами.
Одной из основных химических характеристик металлов является их способность к окислению. Металлы энергично реагируют с кислородом воздуха, образуя оксиды. Это обусловлено тем, что металлы имеют низкую энергию ионизации и могут легко отдавать электроны. Например, железо при взаимодействии с кислородом превращается в ржавчину – оксид железа.
Еще одной важной химической характеристикой металлов является их способность реагировать с кислотами. Металлы образуют соли и выделяются соответствующие ионы в раствор. Например, магний при контакте с соляной кислотой образует хлорид магния и выделяет водород.
Однако не все металлы обладают химическими свойствами, которые были описаны выше. Некоторые металлы, например, золото и платина, являются химически инертными. Они практически не реагируют с кислотами и не окисляются воздухом. Эта свойственная им инертность обусловлена высокой энергией ионизации и слабой степенью активности.
Физические свойства металлов
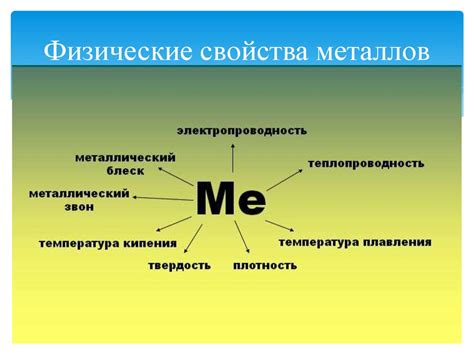
Металлы обладают рядом характерных физических свойств, которые отличают их от других веществ. Одним из таких свойств является высокая теплопроводность. Металлы способны быстро и эффективно проводить тепло, что делает их полезными в различных промышленных процессах и конструкциях. Кроме того, металлы обладают высокой электропроводностью, что позволяет им использоваться в производстве электрических проводов и контактов.
Еще одной важной физической характеристикой металлов является их пластичность. Металлы способны быть деформированными без разрушения, что позволяет их легко обрабатывать и использовать в различных конструкциях. Благодаря этому свойству, металлы могут быть прокатаны, вытянуты и расплавлены для создания различных изделий.
Металлы обладают также значительной прочностью. Они способны выдерживать большие нагрузки и сопротивлять разрушению. Более того, металлы обладают устойчивостью к воздействию механических и агрессивных сред. Это делает их надежными и долговечными материалами для строительства и производства.
Некоторые металлы обладают способностью быть магнитными. Они могут притягиваться к магнитным полям или обладать собственным магнитным полем. Это свойство делает металлы полезными в различных устройствах и технологиях, таких как электромагниты и магнитные датчики.
Металлы в химии 9 класса
В химии 9 класса особое внимание уделяется изучению металлов - важной группы химических элементов. Металлы представляют собой вещества с хорошей электропроводностью, благодаря своей структуре и особому строению атомов. Они обладают такими общими свойствами, как высокая теплопроводность и способность отражать свет.
Металлы имеют широкое применение в различных областях жизни человека. Они используются для создания различных материалов, включая металлические сплавы, как например, сталь и алюминий. Металлы также используются в электротехнике, благодаря своей электропроводности. Большая часть металлов является строительными материалами, используемыми для создания разных конструкций.
Кроме того, металлы играют важную роль в химических реакциях. Они могут проявлять свои особенности и вступать в химические соединения. Например, металлы могут образовывать ионы с положительным зарядом, которые способны образовывать соли. Металлические ионы также могут служить катализаторами в химических реакциях, ускоряя процесс окисления или восстановления других веществ.
Одной из важных характеристик металлов является их реакция с кислотами. Многие металлы могут реагировать с кислотами, образуя соли и выделяя водород. Это обусловлено реакцией металлов с водородными ионами в кислотах. При этом, металлы реагируют с разной интенсивностью и скоростью, в зависимости от их химических свойств.
В химии 9 класса изучаются свойства и химические реакции различных металлов, а также их взаимодействие с другими веществами. Таблицы металлов, их свойства и характеристики помогают систематизировать и запомнить эти знания, а также отличить металлы от других элементов.
Таблица свойств металлов
Металлы - это группа веществ, обладающих особыми химическими и физическими свойствами. В таблице ниже перечислены основные характеристики металлов.
1. Проводимость электричества и тепла: металлы хорошо проводят как электричество, так и тепло. Это связано с наличием свободных электронов, которые могут свободно передвигаться внутри металлической решетки.
2. Пластичность и формоизменяемость: металлы можно легко деформировать и изменить форму без разрушения. Они проявляют свойство пластичности и могут быть прокатаны, вытянуты или расплавлены.
3. Механическая прочность: металлы обладают высокой прочностью и могут выдерживать большие механические нагрузки без деформации или разрушения.
4. Блеск и способность к полировке: металлы имеют характерный блеск и могут быть легко полированы, придавая им эстетическую привлекательность.
5. Долговечность: металлы обладают долговечностью и не подвержены разложению под воздействием воды, кислот и других химических веществ.
В таблице можно увидеть основные свойства различных металлов, такие как плотность, точка плавления, электроотрицательность, атомная масса и другие характеристики. Эта информация помогает классифицировать металлы и определить их применение в различных отраслях промышленности и науке.
| Металл | Плотность (г/см³) | Точка плавления (°C) | Электроотрицательность | Атомная масса (г/моль) |
|---|---|---|---|---|
| Железо (Fe) | 7.87 | 1538 | 1.83 | 55.85 |
| Медь (Cu) | 8.96 | 1083 | 1.90 | 63.55 |
| Алюминий (Al) | 2.70 | 660 | 1.61 | 26.98 |
| Свинец (Pb) | 11.34 | 327 | 2.33 | 207.2 |
Приведенные данные являются лишь примером и не исчерпывают полный список химических элементов и их свойств. Однако они показывают разнообразие свойств и характеристик металлов, которые делают их особенно важными и полезными материалами в нашей повседневной жизни.
Характеристики металлов
1. Проводимость электричества: Металлы обладают высокой проводимостью электричества. Это связано с наличием полностью заполненной зоны проводимости и свободных электронов.
2. Теплопроводность: Металлы также обладают высокой теплопроводностью, что позволяет им эффективно передавать тепло. Это особенно важно при использовании металлов в различных отраслях промышленности.
3. Пластичность и формоизменяемость: Металлы могут быть легко деформированы при нагревании и обработке. Это связано с наличием слабо связанных межатомных связей, которые позволяют металлам принимать новую форму без разрушения их структуры.
4. Химическая реакционность: Металлы, как правило, активно взаимодействуют с другими веществами, особенно с кислотами и солями. Они способны образовывать ионы металла и выделять водород при реакциях с кислотами.
5. Магнитные свойства: Некоторые металлы обладают магнитными свойствами. Например, железо, никель и кобальт являются ферромагнитными и могут притягиваться к магниту или образовывать магнитное поле.
6. Плотность: Металлы обладают высокой плотностью, что делает их тяжелыми по сравнению с другими материалами. Это часто приводит к их использованию в строительстве и производстве тяжелой промышленности.
7. Окисление: Металлы могут претерпевать процесс окисления, при котором образуются оксиды. Однако, некоторые металлы, такие как золото и платина, очень устойчивы к окислению и сохраняют свой блеск и стабильность на протяжении длительного времени.
Классификация металлов
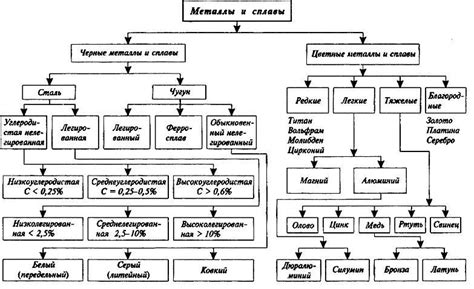
Металлы - это группа химических элементов, которые обладают рядом общих свойств. В зависимости от своих химических свойств, металлы можно классифицировать на основные, щелочные, щелочноземельные и побочные металлы.
1. Основные металлы: Основные металлы включают такие элементы, как железо, медь, цинк, алюминий и т.д. Они обладают хорошей электропроводностью и теплопроводностью, высокой пластичностью и прочностью. Основные металлы обычно встречаются в природе в свободном состоянии и активно используются в промышленности.
2. Щелочные металлы: Щелочные металлы включают такие элементы, как литий, натрий, калий и т.д. Они отличаются высокой химической активностью и реактивностью. Щелочные металлы реагируют с водой, образуя щелочи, и широко используются в производстве щелочей, солей и других химических веществ.
3. Щелочноземельные металлы: Щелочноземельные металлы включают такие элементы, как магний, кальций, стронций и т.д. Они обладают некоторыми химическими свойствами, сходными с щелочными металлами, но менее активными. Щелочноземельные металлы находят широкое применение в производстве различных сплавов, а также используются в химической промышленности и медицине.
4. Побочные металлы: Побочные металлы включают различные элементы, такие как свинец, висмут, марганец и другие. Они обладают различными свойствами и применяются в разных отраслях промышленности. Побочные металлы могут быть токсичными или иметь специфические свойства, которые делают их полезными для определенных процессов или приложений.
Вопрос-ответ
Что такое металлы?
Металлы - это класс элементов, характеризующихся высокой теплопроводностью, электропроводностью, глянцевым блеском и пластичностью. Они обладают общими свойствами, которые отличаются от свойств других классов элементов, таких как неметаллы и полуметаллы.
Какие основные характеристики свойств металлов?
Основные свойства металлов включают высокую теплопроводность и электропроводность, глянцевый блеск, пластичность, хорошую плавкость и способность образовывать сплавы. Они также обычно имеют высокую плотность и твердость.
Какие элементы относятся к классу металлов?
К классу металлов относятся элементы в левой части периодической таблицы, начиная с лития и заканчивая францием. Это включает металлы щелочных металлов, щелочноземельные металлы, переходные металлы и металлы побочных подгрупп. Также к металлам относятся некоторые элементы из групп побочных подгрупп, такие как алюминий, олово и свинец.
Какие свойства делают металлы химически активными?
Металлы обладают свойством реагировать с другими веществами, образуя соединения. Одной из причин их химической активности является низкая ионизационная энергия, что делает их склонными к потере электронов и образованию положительных ионов. Другой причиной активности является способность металлов образовывать соединения с кислородом, образуя оксиды. Это происходит из-за того, что металлы имеют низкий уровень электроотрицательности по сравнению с кислородом.
Какие металлы имеют самую высокую температуру плавления?
Самую высокую температуру плавления имеют платина и ослабленные металлы - вольфрам и молибден. Температура плавления платины составляет около 1772 градусов Цельсия, вольфрама - около 3410 градусов Цельсия, а молибдена - около 2620 градусов Цельсия.

