Взаимодействие кислот с активными металлами является одной из фундаментальных реакций в химии. В результате этой реакции между кислотой и активным металлом образуется соль и выделяется водород. Уравнение реакции между кислотой и активным металлом можно представить следующим образом: кислота + металл → соль + водород.
Однако, чтобы провести эту реакцию, необходимо учесть несколько закономерностей. Во-первых, кислота должна быть достаточно сильной, чтобы активировать металл. Более сильные кислоты, такие как соляная кислота (HCl) и серная кислота (H2SO4), способны реагировать с более широким спектром активных металлов. Однако более слабые кислоты, такие как уксусная кислота (CH3COOH), могут реагировать только с наиболее активными металлами, такими как цинк (Zn) и алюминий (Al).
Во-вторых, необходимо учесть реакционные условия, такие как температура и концентрация кислоты. Высокая температура и высокая концентрация кислоты могут повысить скорость реакции. Однако, при слишком высоких температурах или концентрациях кислоты, может происходить более интенсивное растворение металла, что может привести к нежелательным побочным реакциям.
Взаимодействие кислоты с активными металлами является важным процессом в химии и имеет широкий спектр применений, включая производство солей, водорода и других химических продуктов. Понимание уравнения реакции и основных закономерностей этого процесса является важным для развития новых методов химического синтеза и оптимизации многих технологических процессов.
Взаимодействие кислоты с активными металлами:
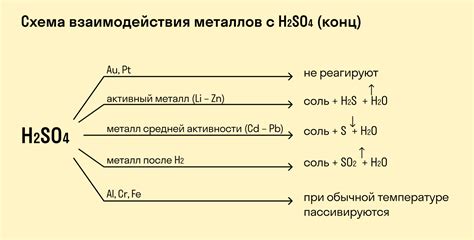
Взаимодействие кислоты с активными металлами является одной из основных реакций, проходящих между веществами в химических системах. Активные металлы обладают высокой химической активностью и способностью образовывать ионы. Кислоты, в свою очередь, представляют собой химические соединения, которые обладают кислотными свойствами и могут отдавать протоны.
При взаимодействии кислоты с активными металлами происходит реакция, в результате которой образуются соли и выделяется водород. Формула общей реакции данного процесса имеет вид: кислота + металл → соль + водород.
Уравнение реакции взаимодействия кислоты с активным металлом может быть записано следующим образом: 2HCl + Zn → ZnCl₂ + H₂. В данном случае кислотой является соляная кислота (HCl), а активным металлом - цинк (Zn).
Взаимодействие кислоты с активными металлами зависит от ряда факторов, включая концентрацию кислоты, вида металла, температуры и давления. Так, активные металлы, такие как калий и натрий, реагируют с кислотами более интенсивно, чем менее активные металлы, например, цинк или алюминий.
Взаимодействие кислоты с активными металлами имеет множество практических применений. Например, процесс, описанный выше, используется в химической промышленности для получения водорода, который затем используется в различных отраслях, включая производство аммиака и рафинирование нефти.
Уравнение реакции
Уравнение реакции между кислотами и активными металлами можно записать в виде:
Кислота + Металл → Соль + Водород
Данный тип реакции является классическим примером химической реакции в химии. В процессе взаимодействия кислоты с активными металлами происходит образование соли и выделение водорода.
Общая схема уравнения реакции выглядит следующим образом:
HA + M → MA + H2
Где HA - формула кислоты, M - металл, MA - соль, H2 - молекула водорода.
Конкретное уравнение реакции будет зависеть от конкретной кислоты и металла, участвующих в реакции. Например, реакция между соляной кислотой и цинком будет выглядеть следующим образом:
HCl + Zn → ZnCl2 + H2
При этом, количество веществ в уравнении должно быть сбалансировано, то есть сумма атомов каждого элемента в реагентах должна быть равна сумме атомов каждого элемента в продуктах реакции.
Основные закономерности
Реакция между кислотой и активным металлом является основной закономерностью взаимодействия этих веществ. При взаимодействии кислоты с активным металлом образуются соли металлов и выделяется водород.
Один из основных примеров такого взаимодействия – реакция между серной кислотой (H2SO4) и цинком (Zn). В результате этой реакции образуется соль цинка и выделяется водород. Уравнение реакции можно записать следующим образом: H2SO4 + Zn → ZnSO4 + H2.
Другой пример – реакция между хлороводородной кислотой (HCl) и магнием (Mg). По аналогии с предыдущим случаем, в результате этой реакции образуется соль магния и выделяется водород. Уравнение реакции можно записать следующим образом: HCl + Mg → MgCl2 + H2.
Важным аспектом взаимодействия кислоты с активными металлами является активность металла. Чем выше активность металла, тем более интенсивной будет реакция с кислотой. Так, натрий (Na) и калий (K) реагируют с водой еще более активно, чем цинк или магний. Поэтому, в контексте взаимодействия с кислотами, калийные или натриевые соли образуются более быстро и энергично.
Влияние окружающей среды
Взаимодействие кислоты с активными металлами зависит от условий окружающей среды. Факторы, такие как температура, давление и наличие других веществ, могут влиять на скорость и направленность реакции.
Известно, что кислоты активно реагируют с металлами, выделяя водород. Однако при повышенных температурах и давлении, такие реакции могут протекать без образования водорода, образуя соединения металла с кислородом из кислоты. Это связано с тем, что при высоких температурах и давлении, кислоты и металлы могут образовывать структуры, которые способствуют интенсивному окислению металла.
Другой фактор, который оказывает влияние на реакцию между кислотой и активным металлом, - наличие других веществ. Например, при наличии кислорода в воздухе, реакция между кислотой и металлом может протекать быстрее и интенсивнее, так как кислород усиливает окислительные свойства кислоты и способствует более эффективному выделению водорода.
Также важно отметить, что растворение металла в кислоте может протекать в соответствии с определенными закономерностями. Например, реактивность металлов в кислотах увеличивается с увеличением их электронной отрицательности и электроотрицательности кислоты.
Следует отметить, что влияние окружающей среды на реакцию кислоты с активными металлами является сложным и может зависеть от конкретной системы и условий эксперимента. Поэтому для изучения таких реакций важно проводить эксперименты в контролируемых условиях и учитывать все факторы окружающей среды.
Практическое применение

Взаимодействие кислоты с активными металлами находит широкое применение в различных областях науки и техники.
В химической промышленности процесс взаимодействия кислоты с активными металлами используется для получения различных промышленных продуктов. Например, реакция соляной кислоты с алюминием приводит к выделению газа водорода, который используется в качестве сырья при производстве аммиака, метанола, синтеза аминов и других компонентов.
Одно из практических применений взаимодействия кислоты с активными металлами - это процесс очистки поверхности металлических изделий от окислов и загрязнений. Например, при использовании соляной кислоты можно удалить окислы железа с поверхности стали, а при взаимодействии с азотной кислотой можно удалить с поверхности цинка окислы и сульфиды. Этот метод широко используется в металлообрабатывающей промышленности.
Кроме того, взаимодействие кислоты с активными металлами применяется в химическом анализе в качестве метода определения содержания металлов в различных материалах. Например, реакция соляной кислоты с металлическим цинком позволяет определить содержание меди в растворах или сплавах.
Вопрос-ответ
Какие активные металлы могут взаимодействовать с кислотами?
С кислотами могут взаимодействовать металлы первой и второй групп периодической системы, такие как литий, натрий, калий, магний, цезий, стронций и др.
Какое уравнение химической реакции между кислотой и активным металлом?
Обычно уравнение реакции между кислотой и активным металлом имеет вид: кислота + металл -> соль + водород. Например, HCl + Zn -> ZnCl2 + H2.
Почему в результате реакции образуется водород?
В результате реакции активного металла с кислотой образуется водород, так как он является продуктом разложения воды.
Что происходит с активным металлом при взаимодействии с кислотой?
При взаимодействии с кислотой активный металл окисляется, отдавая электроны, и вступает в химическую реакцию с кислородом кислоты.
Какова связь между активностью металла и скоростью реакции с кислотой?
Чем активнее металл, тем быстрее протекает реакция с кислотой. Это связано с тем, что активные металлы легче отдают электроны, что ускоряет процесс окисления.
Может ли реакция между кислотой и активными металлами проходить без освобождения водорода?
Нет, взаимодействие кислоты с активными металлами всегда сопровождается выделением газообразного водорода.

