Атомы металлов представляют собой особую группу атомов, обладающих рядом характерных свойств. Они являются основными строительными блоками металлической решетки и отличаются от атомов неметаллов как по электронной структуре, так и по физическим и химическим свойствам.
Одним из основных характерных свойств атомов металлов является наличие малого числа валентных электронов. Обычно атомы металлов имеют один или два валентных электрона, что делает их склонными к потере электронов и образованию положительных ионов. Это обуславливает способность металлов образовывать ионы с положительным зарядом и вступать в реакции с веществами, обладающими отрицательными зарядами.
Кроме того, атомы металлов также обладают высокой электропроводностью. Это связано с наличием свободных электронов в металлической решетке, которые легко перемещаются под действием электрического поля. Именно благодаря этому свойству металлы являются отличными проводниками электричества и тепла.
Еще одним характерным свойством атомов металлов является их способность образовывать сплавы. Металлы могут образовывать твердые растворы с другими металлами, которые могут быть упрочнены путем изменения состава сплава или добавления примесей. Это позволяет получать материалы с различными физическими и механическими свойствами, что является важным фактором их применения в различных отраслях промышленности.
Таким образом, атомы металлов обладают рядом характерных свойств, включая низкое число валентных электронов, высокую электропроводность и способность к образованию сплавов. Они играют важную роль в нашей повседневной жизни и широко используются в различных областях науки и промышленности.
Атомы металлов обладают высокими ионизационными потенциалами
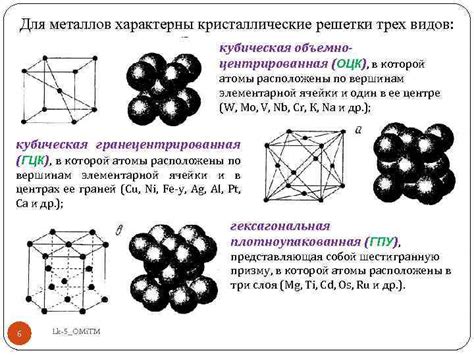
Ионизационный потенциал - это энергия, необходимая для удаления одного электрона из атома. У атомов металлов ионизационные потенциалы обычно являются большими, по сравнению с атомами неметаллов. Это связано с особенностями строения электронных оболочек металлических атомов.
Основная характеристика атома металла - наличие большого числа электронов во внешней электронной оболочке. В результате этого, эти атомы обладают низкой электронной аффинностью, то есть малым энергетическим высвобождением при приобретении нового электрона. Это делает их атомы устойчивыми и способными образовывать положительные ионы.
Высокие ионизационные потенциалы металлических атомов обусловлены сильным взаимодействием электронов с ядром атома. Большая притягательная сила поля ядра делает сложным процесс отрыва электрона от атома металла.
Высокие ионизационные потенциалы металлических атомов оказывают важное влияние на их физические и химические свойства. Они обуславливают высокую температуру плавления и кипения металлов, их хорошую электропроводность и теплопроводность. Также высокий ионизационный потенциал металлов делает их устойчивыми к окислению и взаимодействию с другими веществами.
Металлы образуют положительные ионы
Одной из характерных особенностей атомов металлов является их способность образовывать положительные ионы, утратив один или несколько электронов. Это связано с тем, что атомы металлов имеют малую электроотрицательность, что делает их склонными к отдаче электронов.
Положительные ионы металлов имеют свойства, отличающиеся от нейтральных атомов. Например, благодаря наличию дополнительного положительного заряда, ионы металлов обладают высокой электропроводностью и теплопроводностью. Это особенно важно в промышленности, где металлы широко используются для производства проводов, электрических приборов и других изделий, связанных с электрическими и тепловыми явлениями.
Другим важным свойством положительных ионов металлов является их способность образовывать ионные связи с атомами неметаллов. Такие ионные связи образуют кристаллические структуры, которые обладают высокой прочностью и твердостью. Именно благодаря этим свойствам, металлы широко используются в строительстве, машиностроении, авиации и других отраслях, требующих прочных и долговечных материалов.
Важно отметить, что положительные ионы металлов могут иметь различную валентность, то есть способность отдавать разное количество электронов. Это связано с присутствием в их электронной оболочке нескольких внешних электронов, которые могут быть утрачены в процессе образования ионов. Из-за этого, у металлов может быть несколько ионов с различными зарядами, что определяет их способность образовывать разные соединения и принимать участие в различных химических реакциях.
Атомы металлов имеют малую электроотрицательность
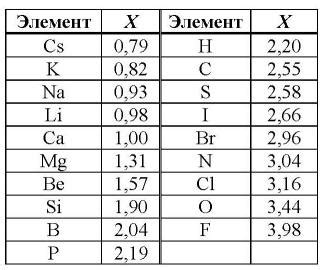
Одним из характерных свойств атомов металлов является их малая электроотрицательность. Электроотрицательность – это способность атома привлекать к себе электроны в химической связи.
Металлы отличаются от не-металлов тем, что имеют низкую электроотрицательность. Это означает, что атомы металлов слабо привлекают электроны и легко отдают их при вступлении в химическую реакцию, образуя положительные ионы – катионы.
Малая электроотрицательность атомов металлов позволяет им образовывать межатомные связи, которые обеспечивают их упорядоченную кристаллическую структуру. Это объясняет металлическую проводимость электричества и тепла у металлов.
Также малая электроотрицательность атомов металлов определяет их химическую активность. Металлы обычно реагируют с не-металлами, отдавая свои электроны и образуя ионы с положительным зарядом.
Важно отметить, что хотя атомы металлов обладают малой электроотрицательностью, в периодической системе они расположены не везде снизу. Например, литий и калий расположены в верхней части первой группы и имеют более высокую электроотрицательность в сравнении с другими металлами.
Металлы хорошие проводники электричества и тепла
Атомы металлов обладают определенными свойствами, которые делают их хорошими проводниками электричества и тепла. В первую очередь, у металлов имеется свободная электронная оболочка, состоящая из отдельных электронов, которые свободно перемещаются между атомами вещества. Это позволяет металлам проводить электрический ток без значительного сопротивления.
Второе свойство, которое делает металлы хорошими проводниками, это их высокая электропроводность. Атомы металлов обладают большим количеством электронов на внешней энергетической оболочке, что способствует свободному движению электронов внутри металлической структуры.
Кроме того, металлы обладают высокой теплопроводностью. Это значит, что они способны передавать тепло эффективно и быстро. Под воздействием нагревания, атомы металлов начинают колебаться и передают это движение близлежащим атомам. Благодаря свободно перемещающимся электронам, передача тепла в металлах происходит очень эффективно.
В результате, благодаря своим свойствам, металлы широко применяются в различных областях: отстройки электрических цепей и проводов до изготовления теплопередающих элементов и радиаторов. Благодаря способности проводить электричество и тепло, металлы играют важную роль в нашей повседневной жизни и промышленности.
Вопрос-ответ
Какие свойства атомов металлов можно назвать характерными?
Характерными свойствами атомов металлов являются: низкая электроотрицательность, большой радиус атома, наличие свободных электронов в валентной оболочке, способность образовывать ионные связи и металлические связи, высокая теплопроводность и электропроводность.
Почему атомы металлов имеют низкую электроотрицательность?
Атомы металлов имеют низкую электроотрицательность из-за своей структуры. У них малое количество электронов в валентной оболочке, что обусловливает их слабое притяжение к электроотрицательным атомам других элементов.
Почему атомы металлов имеют большой радиус?
Атомы металлов имеют большой радиус из-за наличия нескольких энергетических уровней, на которых расположены электроны в их валентной оболочке. Это приводит к увеличению размера атома металла по сравнению с атомами других элементов.
Почему металлы обладают высокой теплопроводностью и электропроводностью?
Металлы обладают высокой теплопроводностью и электропроводностью из-за наличия свободных электронов в их валентной оболочке. Эти свободные электроны свободно передвигаются внутри металлической структуры, перенося тепло и электрический заряд.

