Металлы могут реагировать с кислотами, образуя соли и выделяя газ. Одной из наиболее распространенных кислот, используемой в этих реакциях, является соляная кислота (или хлороводородная кислота).
Соляная кислота (HCl) является сильной минеральной кислотой, которая встречается в природе в виде растворов водорода хлорида. Она используется в различных промышленных и лабораторных процессах, а также в бытовой химии.
В реакциях между металлами и соляной кислотой ион водорода из кислоты замещается металлом, образуя соль и выделяя молекулярный водород. Реакции обычно сопровождаются выделением пузырьков газа и возникновением пени в растворе.
В данной статье рассмотрим 5 уравнений реакции между различными металлами (например, цинком, железом, медью и алюминием) и соляной кислотой. Проследим за изменением раствора и выделением газа, чтобы лучше понять эти реакции.
Уравнение реакции между металлом и соляной кислотой
Металлы являются активными элементами, которые способны взаимодействовать с различными веществами, в том числе с кислотами. Реакция между металлом и соляной кислотой является одной из наиболее простых и широко изученных реакций в химии.
Уравнение такой реакции можно записать в виде: металл + соляная кислота → соль металла + водород. Например, реакция цинка (Zn) с соляной кислотой (HCl) может быть представлена следующим образом: Zn + 2HCl → ZnCl2 + H2.
Процесс реакции между металлом и соляной кислотой можно объяснить следующим образом:
- Соляная кислота является сильным электролитом и, в растворе, отделяется на положительно заряженные ионы водорода (H+) и отрицательно заряженные ионы хлора (Cl-).
- Металл имеет способность отдавать электроны, образуя положительно заряженные ионы металла.
- При соприкосновении металла с соляной кислотой происходит окислительно-восстановительная реакция: металл отдает электроны, переходя в положительно заряженное состояние, а ионы водорода приобретают эти электроны, образуя молекулярный водород (H2).
- Одновременно происходит реакция с формированием соли металла, в случае реакции с соляной кислотой образуется хлорид металла, например, ZnCl2.
Реакция между металлами и соляной кислотой является химической реакцией, которая сопровождается выделением водорода и образованием соли. Она осуществляется при наличии некоторых условий, например, при наличии катализатора или при нагревании. Уравнения реакций между различными металлами и соляной кислотой могут отличаться, в зависимости от активности металла и его реакционной способности.
Реакция между металлом и соляной кислотой
Реакция между металлом и соляной кислотой является примером химической реакции, которая происходит при взаимодействии металлического элемента с соляной кислотой (HCl). В результате такой реакции образуются соли и выделяется водородный газ.
Соляная кислота является одним из наиболее распространенных и известных химических соединений. Она может применяться для различных целей, таких как очистка и удаление загрязнений, а также в качестве исходного вещества для получения других химических соединений.
В отношении реакции с металлами, соляная кислота выступает в роли окислителя, то есть она принимает электроны от металла. При этом металл обладает свойством образования ионов, ионизуясь в растворе.
Реакция между металлом и соляной кислотой может быть представлена уравнением вида:
Металл + соляная кислота → соль + водородный газ
Например, реакция между цинком и соляной кислотой может быть представлена следующим уравнением:
Zn + 2HCl → ZnCl2 + H2
В данной реакции цинк образует ион Zn2+, а соляная кислота образует анион Cl-. В результате образуется соль цинка (цинхлорид) и высвобождается водородный газ.
Такие реакции имеют практическое применение, например, для получения водорода или производства солей. Однако при проведении таких реакций необходимо соблюдать меры предосторожности, так как соляная кислота является ядовитым и опасным веществом.
Каково значение реакции между металлом и соляной кислотой?

Реакция между металлом и соляной кислотой имеет большое значение в химии и промышленности благодаря своим свойствам и применению. Она широко используется для получения солей, очистки и обработки металлических поверхностей, а также в химическом анализе.
Реакция металла с соляной кислотой осуществляется с образованием соответствующего солевого соединения и выделением водорода. В зависимости от свойств металла и концентрации кислоты, реакция может протекать с разной интенсивностью. Некоторые металлы, такие как цинк и железо, обладают достаточной активностью, чтобы реагировать с соляной кислотой при комнатной температуре.
Соли, получаемые в результате реакции металла с соляной кислотой, имеют широкое применение в различных отраслях. Например, хлорид натрия, получаемый при реакции натрия с соляной кислотой, используется в пищевой промышленности, медицине и водоочистке. Карбонат кальция, получаемый при реакции кальция с соляной кислотой, используется в производстве цемента, стекла и множества других материалов.
Реакция металла с соляной кислотой также применяется для очистки и обработки металлических поверхностей. Кислотный раствор используется для удаления окислов и других загрязнений с поверхности металла, что позволяет обеспечить более эффективную сварку, покрытие или другую обработку. Кроме того, реакция металла с соляной кислотой используется в химическом анализе для определения наличия и концентрации металла в образце.
Таким образом, реакция между металлом и соляной кислотой играет важную роль в химии и промышленности. Она позволяет получать соли с различными применениями, использовать кислотные растворы для очистки и обработки металлических поверхностей, а также проводить химический анализ. Это позволяет эффективно использовать ресурсы и обеспечивать качество и надежность производимых изделий и материалов.
Примеры уравнений реакции между металлом и соляной кислотой
Взаимодействие металлов с соляной кислотой является одним из классических примеров химических реакций. Реакция происходит при соприкосновении металла с соляной кислотой, при этом образуются соли и выделяется водородный газ. Реакции данного типа могут быть представлены следующими уравнениями:
- Цинк и соляная кислота:
- Магний и соляная кислота:
- Железо и соляная кислота:
- Алюминий и соляная кислота:
Zn + 2HCl = ZnCl2 + H2↑
Mg + 2HCl = MgCl2 + H2↑
Fe + 2HCl = FeCl2 + H2↑
2Al + 6HCl = 2AlCl3 + 3H2↑
Во всех этих реакциях происходит окислительно-восстановительное взаимодействие металла и кислоты. Металл отдает электроны, образуя положительные ионы, а соляная кислота принимает эти электроны, образуя отрицательные ионы. Результатом реакции является образование соли и выделение водорода.
Таблица ниже содержит примеры уравнений реакций между различными металлами и соляной кислотой, позволяющие увидеть общую закономерность в этих реакциях:
| Металл | Соляная кислота | Соль | Водородный газ |
|---|---|---|---|
| Цинк | HCl | ZnCl2 | H2↑ |
| Магний | HCl | MgCl2 | H2↑ |
| Железо | HCl | FeCl2 | H2↑ |
| Алюминий | HCl | AlCl3 | H2↑ |
Эти примеры показывают, что реакция между металлом и соляной кислотой протекает похожим образом независимо от типа металла. Это явление является следствием общих свойств соляной кислоты и металлов, которые определяют электрохимическую активность их взаимодействия.
Химическая формула реакции между металлом и соляной кислотой
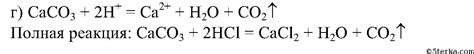
Химическая формула реакции между металлом и соляной кислотой определяется взаимодействием ионов металла с ионами соляной кислоты. Эта формула позволяет описать химический процесс, который происходит при реакции.
Обычно реакция между металлом и соляной кислотой приводит к образованию соли и выделению водорода. Химическая формула такой реакции обычно имеет вид: металл + соляная кислота -> соль + водород.
Для каждого металла существуют определенные условия, при которых происходит реакция с соляной кислотой. Некоторые металлы, такие как железо или алюминий, реагируют с соляной кислотой без нагревания, при комнатной температуре. Другие металлы, например магний или цинк, требуют нагревания для начала реакции.
Химическая формула реакции между металлом и соляной кислотой может быть представлена в виде уравнения, в котором указываются коэффициенты соответствующих веществ. Например, уравнение реакции между цинком и соляной кислотой имеет вид: Zn + 2HCl -> ZnCl2 + H2.
Реакции между металлом и соляной кислотой являются важными в химии и находят применение в различных областях. Эти реакции могут использоваться для получения солей или водорода, а также в процессах очистки и обработки материалов.
Ключевые аспекты реакции между металлом и соляной кислотой
1. Кислотная реакция: Реакция между металлом и соляной кислотой является типичным примером кислотной реакции. Соляная кислота, также известная как хлороводородная кислота, проявляет свойства кислоты, образуя положительные ионы водорода (H+) в растворе. В реакции между металлом и соляной кислотой, ионы водорода обмениваются с металлическими ионами, что приводит к образованию соли и выделению газа водорода.
2. Образование соли: Реакция между металлом и соляной кислотой приводит к образованию соли. Металл реагирует с соляной кислотой, вытесняя из нее водород. Образовавшаяся соль может быть хлоридом металла, если металл принадлежит к группе 1 или 2 (щелочные металлы), или иным солевым соединением, если металл принадлежит к другим группам периодической системы.
3. Выделение водорода: Главным продуктом реакции между металлом и соляной кислотой является выделение водорода. В процессе реакции между ионами водорода и металлическими ионами образуются молекулы водорода (H2), которые вытесняются из раствора в виде газа. Выделение водорода можно наблюдать по появлению пузырьков газа на поверхности металла или в растворе соляной кислоты.
4. Время реакции: Время, необходимое для завершения реакции между металлом и соляной кислотой, может быть различным в зависимости от свойств металла и концентрации соляной кислоты. Некоторые металлы, такие как магний и алюминий, реагируют быстро и эффектно с соляной кислотой, выделяя газ водорода в течение нескольких секунд. Другие металлы могут реагировать медленнее или требовать более концентрированного раствора соляной кислоты.
5. Изменение окраски раствора: При реакции между металлом и соляной кислотой может происходить изменение окраски раствора. Исходным раствором соляной кислоты могут быть безцветные или бледно-желтые жидкости, однако образовавшаяся соль может иметь характерный окрас, например, хлориды меди или железа могут быть синими или зелеными. Изменение окраски раствора может быть использовано в качестве индикатора протекания реакции.
Таким образом, реакция между металлом и соляной кислотой является кислотной реакцией, которая приводит к образованию соли и выделению газа водорода. Она зависит от свойств металла и концентрации соляной кислоты, и может сопровождаться изменением окраски раствора. Изучение этих ключевых аспектов позволяет понять и объяснить основные законы и принципы химических реакций, происходящих между металлами и кислотами.
Факторы, влияющие на скорость реакции между металлом и соляной кислотой

Реакция между металлом и соляной кислотой является одной из наиболее изученных и широко распространенных химических реакций. Скорость этой реакции зависит от различных факторов, которые могут быть физическими или химическими.
Один из основных факторов, влияющих на скорость реакции между металлом и соляной кислотой, - это концентрация кислоты. Чем выше концентрация соляной кислоты, тем быстрее происходит реакция. Это связано с тем, что большее количество активных частиц кислоты обеспечивает более высокую вероятность их столкновения с металлической поверхностью.
Еще одним фактором, влияющим на скорость реакции, является температура среды. При повышении температуры скорость реакции увеличивается, поскольку молекулы обладают бОльшей кинетической энергией и движутся быстрее. Это способствует более интенсивным столкновениям молекул металла и кислоты и увеличивает скорость реакции.
Еще одним фактором, который влияет на скорость реакции, является размер и поверхностная площадь металла. Более мелкие частицы металла имеют большую поверхность, что способствует более активному взаимодействию с кислотой и увеличивает скорость реакции. Также важен и тип металла: некоторые металлы, такие как цинк и железо, более активно реагируют с соляной кислотой, чем другие, например, медь или серебро.
Кроме того, на скорость реакции между металлом и соляной кислотой может влиять наличие катализаторов. Некоторые вещества могут ускорять реакцию, уменьшая энергию активации (пороговую энергию) или предоставляя более удобную поверхность для взаимодействия между металлом и кислотой.
Таким образом, концентрация кислоты, температура, размер и тип металла, а также наличие катализаторов - все эти факторы оказывают влияние на скорость реакции между металлом и соляной кислотой.
Применение реакции между металлом и соляной кислотой в промышленности
Реакция между металлом и соляной кислотой имеет широкое применение в различных отраслях промышленности. Одним из основных назначений этой реакции является получение солей металлов, которые широко используются в различных отраслях.
Прежде всего, реакция между металлом и соляной кислотой используется в процессе производства химических соединений. Путем взаимодействия металла с соляной кислотой можно получить различные соли, которые используются в производстве красителей, пластиков, удобрений и других химических соединений.
Другим важным направлением применения реакции между металлом и соляной кислотой является получение водорода. В процессе реакции образуется водородный газ, который затем может быть использован в таких отраслях, как производство промышленного оборудования, химическая промышленность и энергетика.
Кроме того, реакция между металлом и соляной кислотой широко применяется в процессе очистки и подготовки поверхностей металлических изделий. В результате взаимодействия металла с кислотой происходит удаление окислов, загрязнений и коррозии, что позволяет получить чистую поверхность, готовую к дальнейшей обработке или нанесению покрытия.
Также стоит отметить, что реакция между металлом и соляной кислотой используется в процессе отработки и утилизации отходов. Путем взаимодействия с кислотой металлические отходы превращаются в более безопасные соединения, что позволяет их утилизировать или использовать повторно.
В заключение, реакция между металлом и соляной кислотой имеет широкое применение в промышленности. Она используется для получения солей металлов, производства водорода, обработки поверхностей металлических изделий и утилизации отходов. Эта реакция играет важную роль в различных отраслях промышленности и способствует эффективному использованию ресурсов.
Вопрос-ответ
Какое уравнение реакции между цинком и соляной кислотой?
Цинк и соляная кислота реагируют по следующему уравнению: Zn + 2HCl → ZnCl2 + H2. В результате этой реакции образуется хлорид цинка (ZnCl2) и молекула водорода (H2).
Какие уравнения реакций между разными металлами и соляной кислотой существуют?
Существует несколько уравнений реакций между разными металлами и соляной кислотой. Например, реакция цинка и соляной кислоты: Zn + 2HCl → ZnCl2 + H2. Еще одно уравнение реакции между железом и соляной кислотой: Fe + 2HCl → FeCl2 + H2. Однако, каждое уравнение реакции будет зависеть от конкретных металла и кислоты.
Как происходит реакция между металлом и соляной кислотой?
Реакция между металлом и соляной кислотой заключается в образовании соли и выделении молекулы водорода. Металл с реагирующей кислотой образует солю, в то время как атомы водорода из кислоты соединяются в молекулы и выделяются в виде газа. Это называется общей реакцией основания с кислотой с образованием соли и воды.
Какие металлы реагируют с соляной кислотой?
Металлы, которые реагируют с соляной кислотой, включают цинк (Zn), железо (Fe), медь (Cu), алюминий (Al), никель (Ni), свинец (Pb) и т.д. Эти металлы образуют соли и выделяют молекулы водорода при реакции с соляной кислотой.
Чем обусловлена реакционная способность металлов с соляной кислотой?
Реакционная способность металлов с соляной кислотой обусловлена их электрохимическими свойствами. Металлы, которые находятся выше в ряду реактивности, имеют большую способность вступать в химические реакции. Это связано с их способностью отдавать электроны, образуя положительные ионы. Соляная кислота же, в свою очередь, является сильной кислотой, способной вытеснять другие кислоты из соединений и образовывать соли с металлами.

