Щелочноземельные металлы – это элементы второй группы периодической таблицы Менделеева. В эту группу входят бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Особенностью данных металлов является постепенное снижение температуры плавления по мере движения вверх по группе.
Бериллий, находящийся на верхней ступени группы, обладает наибольшей температурой плавления – около 1287 °С. Данный металл является крайне жестким и легким. Магний, который расположен чуть ниже в группе, имеет температуру плавления уже на 117 °С ниже – около 650 °С. Кальций обладает еще более низкой температурой плавления – примерно 839 °С.
Следующим в группе идет стронций, у которого температура плавления составляет около 769 °С. Барий, находясь на пятом месте группы, имеет еще более низкую температуру плавления – около 727 °С. И, наконец, радий, который расположен на нижней ступени группы, имеет наименьшую величину температуры плавления в группе – около 700 °С.
Таким образом, можно сделать вывод, что температура плавления щелочноземельных металлов прогрессивно снижается по каждой группе – от бериллия до радия. Это свойство является следствием увеличения атомных ионных радиусов и слабости электростатических связей между атомами.
Знание о температуре плавления щелочноземельных металлов имеет важное практическое значение для различных индустриальных процессов, включая литейное производство, производство сплавов и других материалов.
Температура плавления щелочноземельных металлов прогрессивно снижается
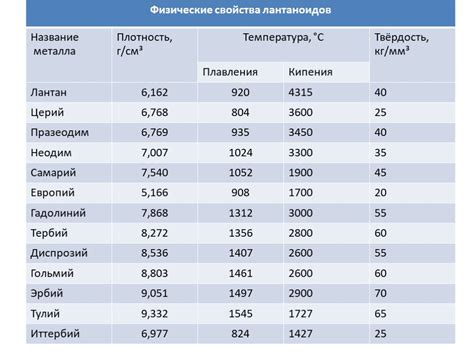
Щелочноземельные металлы - это элементы периодической системы, которые находятся во второй группе и втором периоде таблицы Менделеева. В этой группе находятся бериллий, магний, кальций, стронций, барий и радий. Одной из интересных особенностей этих металлов является их температура плавления.
Температура плавления щелочноземельных металлов прогрессивно снижается по каждой группе. Начиная с бериллия, который имеет самую высокую температуру плавления среди щелочноземельных металлов, по мере перехода к последующим элементам группы, температура плавления снижается.
Магний, расположенный после бериллия, уже имеет более низкую температуру плавления. Кальций, стронций и барий также обладают низкими температурами плавления по сравнению с бериллием.
Наконец, радий, последний элемент группы, имеет самую низкую температуру плавления среди щелочноземельных металлов. Она составляет всего около 700 градусов Цельсия.
Это понижение температуры плавления щелочноземельных металлов связано с постепенным увеличением размера атомов и слабой привлекательной силой между ними. Более крупные атомы имеют более слабую связь, что приводит к более низкой температуре плавления.
Щелочноземельные металлы
Щелочноземельные металлы - это вторая группа элементов периодической таблицы, которая включает бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они отличаются от других металлов своими свойствами и химическими реакциями.
Одной из особенностей щелочноземельных металлов является постепенное снижение температуры плавления с увеличением атомного номера внутри каждой группы. Например, у бериллия температура плавления составляет около 1287°C, в то время как у радия она составляет около 700°C. Это связано с изменением структуры и силы металлической связи в молекулах щелочноземельных металлов.
Щелочноземельные металлы имеют ярко-белый цвет и блестящую поверхность. Они отличаются высокой электропроводностью и теплопроводностью, что делает их полезными в различных промышленных и технических приложениях. Они также реагируют с водой, образуя щелочные растворы и выделяя водород. Это свойство делает их важными для использования в химической промышленности и в производстве водорода.
Щелочноземельные металлы часто используются в различных отраслях, таких как строительство, электроника, авиационная и космическая промышленность. Они также являются важными компонентами в многих минералах и рудах, которые добываются для получения металлов и их соединений.
Температура плавления щелочноземельных металлов
Щелочноземельные металлы - это элементы второй группы периодической таблицы, которые включают бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Отличительной особенностью этих металлов является понижение температуры плавления по каждой группе.
Бериллий является самым тяжелым из всех щелочноземельных металлов и имеет наивысшую температуру плавления - около 1287 градусов Цельсия. За исключением бериллия, остальные щелочноземельные металлы имеют гораздо ниже температуры плавления.
Магний, наиболее распространенный щелочноземельный металл, имеет температуру плавления около 651 градуса Цельсия. Кальций имеет температуру плавления около 839 градусов Цельсия, стронций - около 769 градусов Цельсия, а барий - около 727 градусов Цельсия.
Радий, самый редкий и радиоактивный из щелочноземельных металлов, имеет самую низкую температуру плавления - около 700 градусов Цельсия.
Таким образом, температура плавления щелочноземельных металлов прогрессивно снижается по каждой группе, что связано с увеличением расстояния между атомами и слаблением межатомных связей в соответствующих периодах периодической таблицы.
Снижение температуры плавления
Температура плавления щелочноземельных металлов прогрессивно снижается по каждой группе. Это явление связано с особенностями строения их атомных решеток.
Щелочноземельные металлы представляют собой элементы, расположенные во второй группе основных металлов периодической системы. Известными представителями этой группы являются бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Температура плавления щелочноземельных металлов зависит от удаленности элемента от атомного ядра и энергии, необходимой для разрушения связи между атомами. При увеличении атомного радиуса температура плавления снижается, так как увеличивается межатомное расстояние и слабеют межатомные связи.
Например, бериллий, являющийся первым элементом группы, имеет наивысшую температуру плавления среди щелочноземельных металлов. Его атомный радиус наименьший, и связи между атомами очень прочные. В то же время, радий, последний элемент группы, имеет наименьшую температуру плавления. У него атомный радиус самый большой, и межатомные связи слабее.
Таким образом, снижение температуры плавления щелочноземельных металлов по каждой группе является следствием увеличения атомного радиуса и слабеющих межатомных связей.
Первая группа щелочноземельных металлов

Первая группа щелочноземельных металлов включает в себя бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Эти элементы характеризуются сходными свойствами, такими как низкая плотность и высокая электропроводность.
Температура плавления первой группы щелочноземельных металлов снижается в порядке увеличения атомного номера. Наименьшую температуру плавления имеет бериллий и составляет около 1287 градусов Цельсия. Затем идет магний с температурой плавления около 650 градусов Цельсия, кальций - около 842 градусов Цельсия, стронций - около 777 градусов Цельсия, барий - около 727 градусов Цельсия, и, наконец, радий, температура плавления которого составляет около 700 градусов Цельсия.
Уменьшение температуры плавления щелочноземельных металлов по каждой группе связано с увеличением атомного радиуса и возрастанием межатомных взаимодействий. Это приводит к более слабой связи между атомами и, следовательно, к более низкой температуре, необходимой для разрушения этой связи и перехода в жидкое состояние.
Вторая группа щелочноземельных металлов
Вторая группа щелочноземельных металлов включает кальций (Ca), стронций (Sr) и барий (Ba). Основные свойства этих элементов во многом определяются их электронной конфигурацией, которая обуславливает их химическую активность.
Температура плавления щелочноземельных металлов во второй группе прогрессивно снижается по порядку увеличения атомного номера. Так, кальций имеет наименьшую температуру плавления среди всех трех элементов группы и составляет около 842°C.
Стронций имеет более высокую температуру плавления, которая составляет около 769°C. Барий, самый тяжелый элемент в группе, имеет наиболее высокую температуру плавления среди всех трех элементов и составляет около 727°C.
Прогрессивное снижение температуры плавления щелочноземельных металлов во второй группе объясняется уменьшением межатомного взаимодействия при увеличении размера атомов. Это приводит к снижению прочности межатомных связей и, следовательно, уменьшению энергии, необходимой для разрушения их кристаллической решетки и перехода в состояние плавления.
Третья группа щелочноземельных металлов

В третьей группе щелочноземельных металлов находятся элементы, чья температура плавления прогрессивно снижается по мере увеличения атомного номера. В эту группу входят бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Каждый из этих элементов обладает своими характеристиками и применениями.
Бериллий имеет наиболее высокую температуру плавления в третьей группе – около 1287 градусов Цельсия. Он используется в производстве легких, но прочных сплавов, а также в некоторых ядерных реакторах благодаря своим атомным свойствам.
Магний, с температурой плавления около 650 градусов Цельсия, широко используется в авиационной и автомобильной промышленности из-за своей легкости и прочности. Также магний является важным компонентом в производстве огнепрочных материалов.
Кальций имеет температуру плавления около 842 градусов Цельсия. Этот элемент находит применение в различных отраслях промышленности, включая производство стали, алюминия, цемента и многих других материалов.
Стронций и барий обладают температурами плавления около 769 и 727 градусов Цельсия соответственно. Эти металлы находят применение в производстве специальных сталей, керамических материалов, при производстве стекла и в качестве аддитивов в ядерном энергетическом производстве.
Радий, элемент с наименьшей температурой плавления в группе – около 700 градусов Цельсия, широко известен своим радиоактивным свойством. Из-за его высокой степени радиоактивности он используется в научных и медицинских исследованиях, а также в производстве искусственных источников излучения для радиологической терапии.
Выводы:
Исходя из представленных данных, можно сделать несколько выводов относительно температуры плавления щелочноземельных металлов.
- Общая тенденция: По каждой группе щелочноземельных металлов наблюдается прогрессивное снижение температуры их плавления. Это говорит о том, что с увеличением атомного номера у этих элементов происходит увеличение межатомных расстояний и слабеет связь между атомами, что ведет к понижению точки плавления.
- Образование сплавов: В связи с низкой температурой плавления, щелочноземельные металлы часто используются для создания сплавов с другими металлами. Это позволяет комбинировать их полезные свойства и получать материалы с различными физическими и химическими свойствами.
- Применение в промышленности: Низкая температура плавления щелочноземельных металлов делает их ценным материалом для использования в различных процессах промышленности, особенно в области металлургии и производства аккумуляторов.
Таким образом, знание о температуре плавления щелочноземельных металлов является важным для понимания их свойств и применения в различных областях науки и технологии.
Вопрос-ответ
Почему температура плавления щелочноземельных металлов снижается?
Температура плавления щелочноземельных металлов прогрессивно снижается по каждой группе из-за особенностей строения атомов и их влияния на межатомные взаимодействия. С ростом атомного номера в каждой группе, количество электронов в электронных оболочках увеличивается, что приводит к увеличению силы межатомных связей и понижению температуры плавления.
Какие щелочноземельные металлы имеют наиболее низкую температуру плавления?
Среди щелочноземельных металлов наиболее низкую температуру плавления имеет магний. Его температура плавления составляет около 650 градусов Цельсия. Затем идут кальций, стронций и барий соответственно, у которых температура плавления постепенно увеличивается.
Влияют ли другие факторы, кроме строения атомов, на температуру плавления щелочноземельных металлов?
Да, помимо строения атомов, на температуру плавления щелочноземельных металлов также влияют другие факторы, такие как силы взаимодействия между атомами, структура кристаллической решетки и наличие примесей. Однако строение атомов играет основную роль в определении температуры плавления этих металлов.
Какие еще свойства имеют щелочноземельные металлы?
Щелочноземельные металлы отличаются высокой электропроводностью, низкой твердостью, низким показателем плотности и яркой металлической блеской. Они также реагируют с водой, образуя щелочи и выделяя водород. Эти металлы являются химически активными и энергетически выгодными с точки зрения использования в различных отраслях промышленности.
Какие еще элементы входят в группу щелочноземельных металлов?
В группу щелочноземельных металлов помимо магния, кальция, стронция и бария также входят радий и элементы, которые относят к временным металлам, такие как цирконий и титан. Однако температура плавления у этих элементов отличается от температуры плавления щелочноземельных металлов.

