Реакция цинка с серной кислотой является одной из наиболее распространенных химических реакций. Она широко используется в промышленности и научных исследованиях. Однако, часто требуется ускорить процесс реакции, чтобы получить результаты быстрее или увеличить выход продукта.
Одним из способов ускорить реакцию цинка с серной кислотой является помол металла. Распределение металлических частиц на мельчайшие частицы позволяет увеличить поверхность контакта между металлом и кислотой, что ускоряет протекание химической реакции. Именно поверхность контакта является основным фактором, определяющим скорость реакции в данном случае.
Помол металла осуществляется с помощью специального оборудования, которое разделяет металлические частицы на достаточно мелкие размеры. Это позволяет увеличить поверхность контакта до нескольких десятков и сотен раз, что существенно повышает скорость реакции.
Более того, помол металла также способствует равномерному распределению металлических частиц в кислотной среде, что также ускоряет реакцию. Таким образом, использование помола металла при реакции цинка с серной кислотой позволяет существенно сократить время реакции и повысить выход продукта.
Ускорение химической реакции цинка и серной кислоты

Химическая реакция между цинком и серной кислотой является типичным примером реакции металла с кислотой. При этой реакции образуется сульфат цинка и выделяется водород. Но, вопрос возникает, как можно ускорить данную реакцию?
Один из способов ускорения реакции заключается в помоле цинка перед его реакцией с серной кислотой. При помоле металла увеличивается его поверхностная площадь, что позволяет большему количеству молекул серной кислоты вступить в контакт с цинком и участвовать в реакции. Таким образом, ускоряется химическая реакция.
Кроме того, помол цинка позволяет увеличить скорость реакции за счет уменьшения длины диффузионного пути для частиц серной кислоты к поверхности металла. Благодаря этому увеличивается интенсивность реакции и ускоряется образование продуктов.
Также стоит отметить, что помол цинка оказывает положительное влияние на потоки электронов внутри металла. Это позволяет более эффективно передавать электроны от цинка к серной кислоте и, следовательно, ускоряет реакцию.
Таким образом, помол цинка перед его реакцией с серной кислотой позволяет ускорить химическую реакцию за счет увеличения поверхностной площади металла, уменьшения диффузионного пути для частиц кислоты и повышения эффективности передачи электронов между цинком и серной кислотой.
Металлический цинк: свойства и применение
Цинк – химический элемент из группы переходных металлов периодической системы Менделеева, обозначается символом Zn. Он обладает светло-серым цветом и обнаружился еще в древние времена.
Цинк является довольно пластичным металлом и может быть легко прокатан в листы или протянут в проволоку. Его плотность равна 7,13 г/см³, а точка плавления составляет 419 °C. Цинк активно взаимодействует с кислотами, особенно с соляной и серной кислотами, с выделением водорода и образованием соответствующих солей.
Применение цинка в различных отраслях промышленности очень широко. Благодаря своим антикоррозионным свойствам, цинк используется для покрытия металлических поверхностей, чтобы предотвратить их ржавление. Также, цинк используется в производстве аккумуляторов, цинковых сплавов, косметических продуктов, красок и пигментов, обуви и многих других товаров.
В лабораторных условиях цинк может использоваться при проведении химических экспериментов, включая реакцию с серной кислотой. При помоле металла, ускоряется скорость реакции, освобождается больше водорода и выделяется больше тепла.
Химическая реакция между цинком и серной кислотой
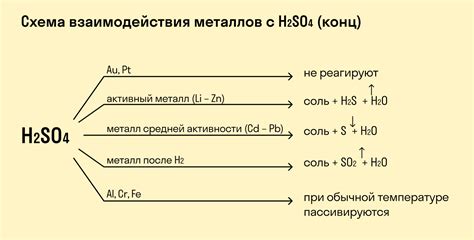
Химическая реакция между цинком и серной кислотой является классическим примером реакции металла с кислотой. Эта реакция является экзотермической, то есть сопровождается выделением тепла.
Цинк реагирует с серной кислотой с образованием соли цинка и выделением водорода. Уравнение реакции выглядит следующим образом:
Zn + H2SO4 → ZnSO4 + H2
В этой реакции ион цинка, Zn2+, обменивается своими двумя электронами с лежащими в серной кислоте водородными ионами, H+. Результатом этого обмена является образование соли цинка, ZnSO4, и молекулы водорода, H2.
Серная кислота, H2SO4, является одним из самых сильных минеральных кислот и хорошо реагирует с большинством металлов. Реакция с цинком может протекать при комнатной температуре с достаточно высокой скоростью, особенно при помоле металла.
Ускорение реакции цинка с серной кислотой при помоле металла объясняется увеличением поверхности контакта между цинком и кислотой. При помоле металла его поверхность становится более мелкой и активной, что способствует более интенсивному протеканию реакции и увеличению выделения водорода.
Влияние помола цинка на скорость реакции
Помол цинка играет важную роль в скорости реакции с серной кислотой. Чем мельче металл, тем большую площадь поверхности он предоставляет для реакции. Это позволяет воде лучше взаимодействовать с цинком и ускоряет процесс химической реакции.
Когда цинк помолот до мелкого состояния, поверхность его частиц увеличивается, что приводит к повышению активности металла. Мельче помолотый цинк имеет большую доступность для серной кислоты, большую площадь поверхности для контакта с кислотой, что увеличивает количество реагирующих частиц и, соответственно, увеличивает скорость реакции.
Другими словами, помол цинка ускоряет реакцию с серной кислотой, так как предоставляет больше поверхности для взаимодействия между металлом и кислотой.
Также стоит упомянуть, что помол цинка может увеличить температуру реакции, так как в процессе помола частицы металла приходят в более активное состояние и обладают более высокой энергией. Повышение температуры способствует быстрому перемешиванию молекул и повышению их скорости, что в результате ускоряет химическую реакцию цинка с серной кислотой.
Важно отметить, что помол цинка необходимо проводить в специальном оборудовании с соблюдением всех безопасных правил и мер предосторожности, так как металлические порошки могут быть опасны для человека при вдыхании или контакте с кожей.
Получение порошкообразного цинка для ускорения реакции

Ускорение реакции цинка с серной кислотой может быть достигнуто путем использования порошкообразной формы металла. Порошкообразный цинк имеет более высокую поверхностную активность, что увеличивает скорость взаимодействия с реагентами и дает возможность более эффективного использования химической энергии.
Получение порошкообразного цинка может быть осуществлено различными способами. Один из них - механическое помоление металла. Для этого цинк может быть подвергнут измельчению в специальных шаровых мельницах или вибрационных мельницах. Результатом такого помола является образование мелких частиц цинка размером около нескольких микрометров.
Мельчение цинка приводит к увеличению его поверхности, что, в свою очередь, способствует более быстрой и интенсивной реакции с серной кислотой. Мелкие частицы цинка имеют большую площадь контакта с реагентами, что обеспечивает эффективное протекание процесса. Кроме того, порошкообразная форма цинка легче смешивается с серной кислотой и обеспечивает равномерное распределение реагентов.
Использование порошкообразного цинка в реакции с серной кислотой позволяет значительно сократить время необходимое для завершения процесса. Этот факт является важным при производстве и применении различных химических продуктов, где существенными параметрами являются скорость реакции и эффективность использования реактивов.
Окисление цинка и выделение сероводорода
Окисление - это процесс химической реакции, при котором вещество теряет электроны. Взаимодействие цинка с серной кислотой приводит к окислению цинка и образованию ионов цинка.
В результате реакции цинк вступает в химическую связь с серной кислотой, при этом происходит перенос электронов от цинка к серной кислоте. В результате окисления цинка и снижения валентности атомов цинка происходит выделение сероводорода.
Сероводород - это химическое вещество с характерным запахом гнилого яйца. Он образуется в результате химической реакции между цинком и серной кислотой. Сероводород является ядовитым газом и может быть опасным для здоровья человека.
Для ускорения реакции цинка с серной кислотой можно использовать помол металла. Более мелкие частицы цинка имеют большую поверхность взаимодействия с серной кислотой, что способствует более быстрой реакции и большему выделению сероводорода. Помол цинка также позволяет получить более равномерное и эффективное окисление металла.
Таким образом, окисление цинка и выделение сероводорода при взаимодействии с серной кислотой является химической реакцией, которая может быть ускорена помолом металла. Выделение сероводорода является важным аспектом данной реакции, и его образование может быть использовано в различных процессах и технологиях.
Термохимические аспекты реакции цинка с серной кислотой

Реакция цинка с серной кислотой является эндотермическим процессом, в результате которого образуется сульфат цинка и выделяется газообразный водород. Этот процесс активно применяется в химическом производстве и сфере научных исследований.
Одним из важных термохимических аспектов этой реакции является теплореактивность. В процессе взаимодействия цинка с серной кислотой происходит поглощение тепла, что свидетельствует о эндотермическом характере реакции. Это означает, что какая-то часть энергии, необходимая для протекания реакции, поставляется из окружающей среды.
Термохимические данные позволяют оценить теплоэффект реакции цинка с серной кислотой. Известно, что стандартная энтальпия образования сульфата цинка равна ΔH⁰ = -674 kJ/mol, а стандартная энтальпия образования воды составляет ΔH⁰ = -285.83 kJ/mol. Исходя из этих данных, можно сделать вывод о выделении значительного количества тепла в процессе реакции цинка с серной кислотой.
Следует отметить, что термохимические свойства реакции цинка с серной кислотой могут варьироваться в зависимости от условий протекания процесса. Например, при изменении концентрации серной кислоты или температуры, может измениться теплореактивность и скорость реакции. Такие изменения позволяют регулировать энергетические характеристики реакции с целью оптимизации технологических процессов.
Применение ускоренной реакции цинка и серной кислоты
Ускоренная реакция цинка и серной кислоты является важным процессом в химической промышленности и научных исследованиях. Эта реакция применяется для получения различных химических соединений и использования их в различных сферах деятельности.
Цинк и серная кислота взаимодействуют, образуя сульфат цинка и выделяя водород. Ускорение этой реакции достигается путем помола металла, что позволяет повысить скорость контакта между частицами цинка и серной кислоты. Более тонкое помоление металла обеспечивает более равномерное распределение цинка в серной кислоте и увеличивает площадь поверхности контакта, что приводит к увеличению скорости реакции.
Применение ускоренной реакции цинка и серной кислоты находит широкое применение в различных сферах. Например, в химической промышленности эта реакция используется для получения сульфата цинка, который является важным компонентом в производстве гальванических покрытий, удобрений, пигментов и других химических соединений.
Кроме того, ускоренная реакция цинка и серной кислоты используется в аналитической химии и научных исследованиях. Она позволяет получать высокочистые образцы цинка для дальнейшего анализа и использования в различных экспериментах и исследованиях.
Также стоит отметить, что ускоренная реакция цинка и серной кислоты является безопасным и экологически чистым процессом. В процессе реакции не выделяются вредные вещества или газы, что делает ее применение безопасным для окружающей среды.
Вопрос-ответ
Какое вещество образуется при реакции цинка с серной кислотой?
При реакции цинка с серной кислотой образуется сульфат цинка и выделяется водород.
Почему реакция цинка с серной кислотой ускоряется при помоле металла?
При помоле металла увеличивается его поверхность контакта с кислотой, что позволяет молекулам кислоты более эффективно сталкиваться с атомами цинка. Это приводит к увеличению скорости реакции.
Какие факторы могут влиять на скорость реакции цинка с серной кислотой?
На скорость реакции цинка с серной кислотой могут влиять факторы, такие как концентрация кислоты, температура окружающей среды, размер и форма цинка, наличие катализаторов и т.д.
Какие основные свойства у серной кислоты?
Серная кислота (H2SO4) является одним из наиболее распространенных химических соединений. Она обладает высокой коррозионной активностью, является сильной дигидратирующей и окислительной кислотой, обладает свойством образовывать соли (сульфаты) с различными металлами. Также она является одним из основных промышленных химических соединений и широко применяется в различных отраслях промышленности и научных исследованиях.
Что такое молекулярная формула цинка?
Молекулярная формула цинка - Zn. Цинк - это химический элемент с атомным номером 30. Он является серебристо-белым металлом, обладает хорошей термической и электрической проводимостью, и широко применяется в промышленности, особенно в производстве сплавов и как защитное покрытие для других металлов.
