В химических процессах металлы могут быть получены путем восстановления их оксидов с использованием угля в качестве восстановителя. Этот метод является одним из наиболее распространенных и эффективных способов получения металлов.
Уравнения реакций, описывающих процесс восстановления оксидов металлов углем, подтверждаются экспериментальными данными и позволяют определить не только стехиометрический коэффициент, но и энергетический эффект данной реакции. В результате процесса восстановления металлов оксид углерода окисляется до диоксида углерода, а металлы образуются в виде элементарных веществ.
Примером реакции восстановления металла оксидом углем может быть реакция восстановления оксида железа (III) (Fe2O3) углем (С). Уравнение реакции выглядит следующим образом:
Fe2O3 + 3C → 2Fe + 3CO
Таким образом, в результате восстановления оксида железа (III) углем образуется чистый железо и углеродный оксид (CO). Этот процесс широко применяется в промышленности для получения чистого железа, используемого в производстве стали.
Понятие и основной принцип получения металлов
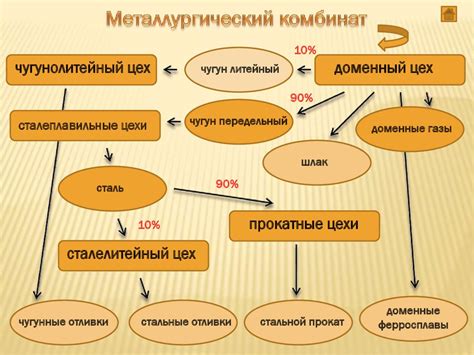
Получение металлов является одной из ключевых задач в химии и металлургии. Металлы широко используются во многих отраслях промышленности и играют важную роль в различных технологических процессах. Одним из основных методов получения металлов является их восстановление из соединений, особенно оксидов, при помощи угля или других восстановителей.
Основной принцип получения металлов при восстановлении их оксидов углем заключается в использовании углерода в качестве сильного восстановителя. Уголь обладает высокой активностью и способен отдавать свои электроны металлу, в результате чего оксид металла превращается в металл. Этот процесс называется редукцией.
Восстановление металлов углем может проводиться как на промышленном уровне, так и в лабораторных условиях. Для этого сначала приготавливают смесь оксида металла и угля, затем нагревают ее до определенной температуры и поддерживают в течение определенного времени. В результате происходит реакция восстановления, в результате которой оксид превращается в чистый металл.
Процесс получения металлов при восстановлении их оксидов углем имеет ряд преимуществ. Во-первых, уголь - дешевый и широко доступный восстановитель, что делает этот метод экономически выгодным. Во-вторых, редукция оксидов углем происходит при достаточно низких температурах, что позволяет снизить энергозатраты на процесс. Кроме того, этот метод позволяет получать металлы высокой степени чистоты.
Однако, восстановление металлов углем имеет и некоторые ограничения. Некоторые оксиды металлов могут быть сложно восстановлены углем из-за высокой термической стабильности. Кроме того, в процессе восстановления может образовываться значительное количество нежелательных продуктов, таких как окислы углерода или неочищенный металл. Поэтому, перед использованием данного метода необходимо тщательно изучить его условия и возможности.
Уравнения реакций получения металлов
Металлы являются важными и широко используемыми материалами в различных отраслях промышленности. Открытие процессов получения металлов из их руд или оксидов было важным шагом в развитии человечества.
Одним из методов получения металлов является их восстановление из оксидов углем. Восстановление оксидов металлов происходит в результате реакции между металлическими оксидами и углеродом при высоких температурах.
Например, восстановление оксида железа(III) углеродом порождает реакцию:
Fe2O3 + 3C → 2Fe + 3CO
где Fe2O3 - оксид железа(III), C - углерод, Fe - полученный металлический железо, CO - образующийся углекислый газ.
Аналогично, восстановление оксида цинка углеродом порождает реакцию:
ZnO + C → Zn + CO
где ZnO - оксид цинка, C - углерод, Zn - полученный металлический цинк, CO - образующийся углекислый газ.
- Другим важным процессом получения металлов является их выделение из растворов в виде соединений. Например, получение меди происходит из ее сульфатного раствора путем электролиза.
- Еще одним способом получения металлов является восстановление их из солевых растворов с помощью других металлов. Например, получение цинка из его сульфатного раствора можно осуществить путем внедрения в него алюминия, что приводит к реакции восстановления и образованию металлического цинка и алюминиевого сульфата.
Вопрос-ответ
Какие металлы могут быть получены путем восстановления их оксидов углем?
Путем восстановления оксидов углем можно получить металлы, такие как железо, медь, свинец, цинк, никель, кобальт, марганец и др. Уголь служит в этом процессе в качестве восстановителя, способного снижать оксиды металлов до их элементарных состояний.
Какие уравнения можно использовать для описания реакции получения металлов оксидов углем?
Уравнения для описания реакции получения металлов оксидов углем зависят от конкретного металла и его оксида, но обычно включают в себя восстановление оксида углем и образование металлического элемента и углекислого газа. Например, для восстановления оксида железа (Fe2O3) углем (C) можно использовать следующую реакцию: Fe2O3 + 3C → 2Fe + 3CO.
Какие условия необходимы для проведения реакции получения металлов оксидов углем?
Для проведения реакции получения металлов оксидов углем необходимо наличие оксидов металлов, угля в качестве восстановителя, а также определенных температуры и условий окружающей среды. Точные условия зависят от конкретного металла и его оксида, но в общем случае требуется высокая температура и отсутствие кислорода, чтобы избежать окисления металлического элемента.
Какую роль играет уголь в реакции получения металлов оксидов углем?
Уголь играет роль восстановителя в реакции получения металлов оксидов углем. Он содержит углерод, который способен взаимодействовать с кислородом в оксиде металла, снижая его до элементарного состояния. Уголь окисляется при этом процессе, образуя углекислый газ. Таким образом, уголь служит ключевым компонентом в реакции получения металлов оксидов углем.