Щелочные металлы - это элементы, которые принадлежат к первой группе периодической системы: литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они являются самыми реакционными и химически активными металлами, обладают хорошей проводимостью тепла и электричества.
Один из способов получения щелочных металлов - это электролиз. Электролиз выполняют в расплавах солей щелочных металлов при применении постоянного электрического тока. Расплавы солей представляют собой ионные жидкости, состоящие из положительных и отрицательных ионов.
Процесс электролиза щелочных металлов основан на преобразовании энергии электрического тока в химическую энергию. Под действием электрического тока положительные ионы металлов (катионы) перемещаются к отрицательному электроду (катоду), а отрицательные ионы (анионы) перемещаются к положительному электроду (аноду). В результате процесса на катоде образуется металлический осадок, который можно легко извлечь.
Электролиз щелочных металлов - это источник получения чистых металлов с высокой степенью чистоты и позволяет контролировать химический состав продукта. Данный метод широко применяется в промышленности для получения щелочных металлов, которые находят широкое применение в различных отраслях науки и техники.
Процесс получения щелочных металлов
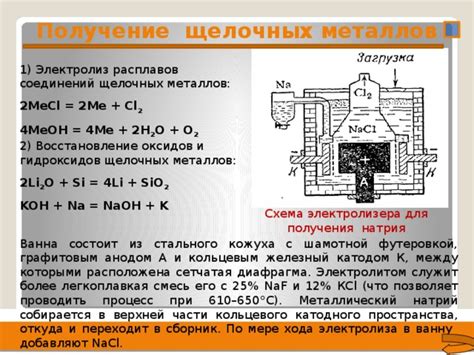
Щелочные металлы, такие как литий, натрий и калий, получаются с помощью электролиза их соединений. Один из основных способов получения щелочных металлов - электролиз плавящихся солей.
Для начала процесса получения щелочных металлов необходимы специальные электролизные ячейки. В этих ячейках находятся два электрода - анод и катод. Анод изготавливают из инертного материала, такого как платина, чтобы он не реагировал с веществами, а катодом обычно служит металлическая сетка или пластины из щелочного металла.
В электролизной ячейке в качестве электролита используют плавящиеся соли щелочных металлов. Плавящиеся соли обеспечивают достаточную подвижность ионов в растворе. При подключении источника тока к аноду и катоду, начинается электролиз.
При электролизе плавящейся соли, ионы металла смещаются к катоду, где происходит их отрицательная редукция. Таким образом, щелочные металлы осаждаются на катоде. Анод, в свою очередь, обеспечивает течение электролитической реакции с положительным ионом.
Получение щелочных металлов методом электролиза имеет ряд преимуществ. Во-первых, электролиз позволяет получить щелочные металлы с высокой степенью чистоты. Во-вторых, данный метод позволяет получать щелочные металлы большими объемами и на промышленной основе. Это делает процесс электролиза эффективным и экономически выгодным способом получения щелочных металлов.
Метод электролиза в получении щелочных металлов
Электролиз является эффективным методом получения щелочных металлов, таких как натрий и калий. Этот процесс основан на использовании электрического тока для разложения соединений металла и их превращения в металлическую форму.
Для проведения электролиза требуется специальная ячейка, называемая электролитической ячейкой. В этой ячейке размещаются два электрода - катод и анод. Катодом служит металлическая пластина или сетка, на которой происходит осаждение металла, а анодом - инертный материал, например, платиновая пластина.
В ходе электролиза, в электролитической ячейке растворяют специальные соли щелочных металлов. Когда подводится электрический ток к ячейке, происходит разложение этих солей на положительно заряженные катионы и отрицательно заряженные анионы.
Положительно заряженные катионы мигрируют к катоду и осаждаются на его поверхности в виде металла. Например, в случае с натрием, ионы Na+ притягиваются к катоду, где принимают электроны и образуют металлический натрий. Анионы же, такие как OH-, набираются положительного заряда на аноде и участвуют в реакциях окисления.
Электролиз щелочных металлов широко применяется в производстве промышленных масштабов. Он позволяет получать чистые и высококачественные металлы с минимальным количеством примесей. Помимо этого, электролиз также является экологически более безопасным методом получения металлов по сравнению с другими процессами.
Преимущества электролиза при получении щелочных металлов

Электролиз является одним из основных и наиболее эффективных методов получения щелочных металлов, таких как литий, натрий и калий. Этот процесс основан на использовании электрического тока для разложения электролита, содержащего соответствующие соединения металлов, на ионы металла и отрицательные ионы.
Одним из главных преимуществ электролиза является его высокая эффективность и точность в получении чистого щелочного металла. Электролиз позволяет удалить примеси и нечистоты из исходного материала, что обеспечивает высокую степень очистки и повышает качество полученного металла.
Электролиз также отличается высокой степенью контроля и регулировки процесса получения металла. Путем изменения напряжения, тока и других параметров процесса можно достичь нужных характеристик получаемого металла, таких как его чистота, размер, форма и структура. Это позволяет адаптировать процесс получения металла под конкретные требования и нужды промышленности.
Еще одним преимуществом электролиза является его экономическая эффективность. Несмотря на то, что этот процесс требует электрической энергии, его высокая эффективность, возможность использования рециклируемых материалов и минимальные потери делают его выгодным с точки зрения затрат. Кроме того, электролиз может быть масштабирован для промышленного применения и может быть осуществлен на крупных масштабах производства.
Таким образом, электролиз является важным и эффективным методом получения щелочных металлов, обладающим рядом преимуществ, включая высокую степень очистки, контроля и регулировки процесса, а также экономическую эффективность. Это делает его необходимым инструментом в производстве щелочных металлов для многих отраслей промышленности.
Практическое применение полученных щелочных металлов
Натрий и калий — два самых распространенных щелочных металла, получают широкое применение в различных отраслях промышленности.
Натрий используется в производстве мыла, стекла, щелочных накаливаемых ламп, а также в пищевой промышленности для консервирования пищевых продуктов.
Калий нашел применение в сельском хозяйстве, где используется в качестве удобрения для повышения плодородия почв, а также для синтеза калийных удобрений.
Благодаря своим химическим свойствам, щелочные металлы также нашли применение в химической промышленности. Например, калий используется в производстве каустической соды, гидроксида калия и калийных солей, которые широко применяются в производстве стекла, мыла и других химических продуктов.
Литий, еще один щелочной металл, нашел свое применение в производстве литиевых батарей. Эти мощные и легкие батареи используются в различных устройствах, таких как мобильные телефоны, ноутбуки, электрические автомобили и дроны.
Также литий применяется в производстве керамики и стекла высокой прочности, а также в фармацевтической промышленности для синтеза лекарственных препаратов.
Вопрос-ответ
Какие щелочные металлы можно получить с помощью электролиза?
С помощью электролиза можно получить щелочные металлы, такие как литий, натрий, калий, рубидий и цезий.
Чем особенно полезен электролиз для получения щелочных металлов?
Электролиз является эффективным методом для получения щелочных металлов, так как позволяет получать их в очень высокой чистоте и больших количествах. Более того, электролиз позволяет получать металлы из их соединений, что делает этот метод экономически выгодным.
Как происходит процесс электролиза для получения щелочных металлов?
В процессе электролиза для получения щелочных металлов используется техника, называемая "расплавленные соли". Соль щелочного металла (например, хлорид натрия) нагревают до состояния расплава, а затем проходит электрический ток через этот расплав. Под воздействием тока происходит разложение соли на ионы металла и ионы отрицательного элемента. Ионы металла осаждаются на отрицательном электроде (катоде), а ионы отрицательного элемента на положительном электроде (аноде). Таким образом, на катоде выпадает металл, в нашем случае щелочный металл.
Какие условия необходимы для успешного проведения электролиза и получения щелочных металлов?
Для успешного проведения электролиза и получения щелочных металлов необходимо соблюдать несколько условий. Во-первых, нужно использовать достаточно высокую температуру, чтобы соль щелочного металла стала расплавленной. Во-вторых, нужно обеспечить создание электрической цепи, через которую будет проходить ток. Для этого требуется использовать два электрода, один из которых будет положительно заряженным (анод), а другой - отрицательно (катод). Наконец, важно использовать соль, содержащую щелочный металл, так как именно она будет разлагаться при электролизе.
