Атомы металлов играют важную роль во многих сферах нашей жизни, таких как машиностроение, электроника, химия и др. Одной из причин, почему атомы металлов так широко используются, является их способность легко отдавать электроны.
Отдача электронов является ключевым свойством металлов и обуславливается специфической структурой и свойствами их атомов. Металлические атомы имеют, как правило, относительно небольшое количество электронов во внешнем электронном слое, так называемом валентном слое.
Валентный слой атома металла может содержать от 1 до нескольких электронов. Поскольку электроны представляют собой заряженные частицы, они могут легко перемещаться между атомами металла, образуя так называемую "электронную оболочку". Электронная оболочка может быть описана как область, в которой электроны находятся, а также их поведение в данной области.
Перемещение электронов между атомами металла происходит благодаря наличию свободных электронов в валентном слое. Свободные электроны являются электронами, которые не связаны с определенным атомом, а подвижность этих электронов создает электрическую проводимость металлов.
Таким образом, причинами легкой отдачи электронов атомами металлов являются их структура, наличие свободных электронов в валентном слое и возможность электронов перемещаться между атомами.
Механизм отдачи электронов металлами
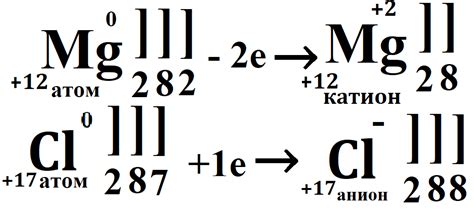
Металлы, благодаря своей электропроводности, способны легко отдавать электроны. Рассмотрим механизм этого процесса.
В атоме металла электроны находятся в энергетических уровнях, которые образуют энергетическую зону. Валентные электроны занимают нижние энергетические уровни, близкие к ядру атома. Эти электроны слабо связаны с ядром и могут легко перемещаться внутри металлической структуры.
При воздействии внешнего электрического поля на металл, происходит смещение электронов. Изменение энергетического состояния электронов влечет за собой их перемещение. Электрическое поле направляет движение электронов, благодаря чему они начинают двигаться в определенном направлении.
Легкость отдачи электронов металлами объясняется их свойствами. У металлов низкая электроотрицательность, что делает их способными отдавать электроны. Кроме того, в металлах наличие свободных электронов позволяет им легко перемещаться и создавать электрический ток.
Все эти факторы делают металлы хорошими проводниками электричества и отличают их от неметаллов, у которых отдача электронов происходит с большими трудностями.
Причины легкой отдачи электронов атомами металлов
Отдача электронов атомами металлов является важным физическим явлением, которое возникает в результате взаимодействия электронов с внешними электромагнитными полями или другими частицами. Причины, по которым атомы металлов легко отдают электроны, включают следующие:
- Широкая зона проводимости: В металлах образуется широкая зона проводимости, что означает, что электроны могут свободно двигаться по всему обьему материала.
- Малая энергия ионизации: Атомы металлов имеют обычно малую энергию, необходимую для удаления одного электрона из валентной оболочки. Это позволяет легко отдать электроны и образовать положительные ионы.
- Низкая аффинность к электрону: Металлы обладают низкой аффинностью к электрону, что означает, что они не сильно притягивают дополнительные электроны и не тянут их в свои оболочки. Это способствует легкой отдаче электронов.
- Металлический связной характер: В металлах электроны образуют свободное электронное облако, которое может двигаться вдоль кристаллической решетки без существенного сопротивления. Это облегчает отдачу электронов при взаимодействии с внешними электрическими полями или другими частицами.
- Эффекты поверхности: Поверхность металлов может обладать особыми физико-химическими свойствами, которые способствуют легкой отдаче электронов. Например, на поверхности металлов могут образовываться малочисленные зоны с восстановленной структурой, где электроны могут свободно двигаться и отдаваться.
В целом, причины легкой отдачи электронов атомами металлов объясняются их особыми физическими и химическими свойствами, которые делают их электронно-активными и способными свободно обмениваться частицами с окружающей средой.
Различия между атомами металлов и другими элементами
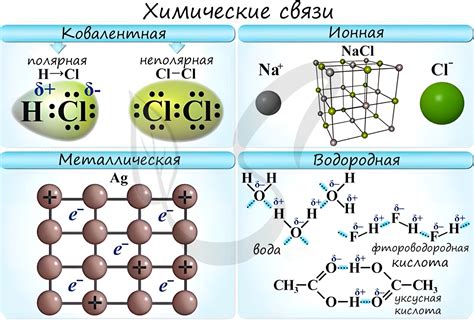
1. Структура атомов: Атомы металлов имеют особую структуру, которая делает их уникальными по сравнению с другими элементами. В отличие от атомов неметаллов, атомы металлов имеют малое количество валентных электронов, что является основной причиной их легкой отдачи при взаимодействии с другими атомами.
2. Зона проводимости: У атомов металлов электроны в зоне проводимости имеют большую подвижность. Это происходит из-за особенной геометрии и связи электронов внутри атома. У других элементов, таких как неметаллы, полупроводники или изолирующие материалы, электроны в зоне проводимости обладают меньшей подвижностью.
3. Электронная структура: У атомов металлов электроны могут перемещаться с одной орбиты на другую, образуя так называемую "оболочку свободных электронов". Это позволяет атомам металлов легко отдавать электроны при взаимодействии с другими атомами и веществами. В то же время, у атомов других элементов электроны имеют более сложную и закрытую структуру, что затрудняет их отдачу.
4. Межатомные связи: Силы межатомных связей в металлах обычно слабее, чем в других элементах. Это объясняется тем, что электроны в металлах могут легко перемещаться внутри кристаллической решетки, образуя электронную газовую модель. Поэтому атомы металлов имеют меньшие энергии связи и более слабые притяжения к другим атомам или ионам.
Таким образом, различия в структуре атомов, зоне проводимости, электронной структуре и межатомных связях делают атомы металлов особенными и способными к легкой отдаче электронов при взаимодействии с другими веществами.
Эффекты отдачи электронов
1. Вероятность рассеяния электронов
При взаимодействии электронов с атомами металла существует вероятность их отклонения от первоначального направления движения. Это связано с тем, что атомы металла являются неоднородными средами, где сосуществуют атомные ядра и электроны. В результате столкновения электрона с атомом, электрон может быть рассеян в другом направлении, в зависимости от среднего взаимодействия с атомами металла.
2. Ионизация атома металла
При отдаче электронов атомы металла могут также ионизироваться, т.е. терять один или несколько электронов. Ионизация происходит в результате взаимодействия вылетевшего электрона с другими электронами в атоме металла или с атомами других веществ, находящихся на поверхности материала. Этот процесс, помимо отдачи электрона, приводит к изменению заряда атома металла и возникновению заряженных частиц.
3. Поляризация атомов металла
Отдача электронов атомами металла может также вызывать эффект поляризации, т.е. изменение распределения зарядов в атоме металла. Под действием внешнего электрического поля ионизованный атом металла приближается к электроду, что значительно влияет на направление движения электрона и его энергию. Этот процесс может приводить как к усилению отдачи электронов, так и к ее ослаблению, в зависимости от условий среды и характера взаимодействия.
4. Рассеяние электронов на поверхности металла
При приходе на поверхность металла электроны могут также рассеиваться в зависимости от поверхностных свойств материала. Рассеяние электронов может быть вызвано как дефектами поверхности (неровности, порами и т.д.), так и взаимодействием с другими атомами или молекулами, оказывающими влияние на преломление или отражение электронов.
Вопрос-ответ
Чем обусловлена легкая отдача электронов атомами металлов?
Легкая отдача электронов атомами металлов обусловлена их особенной электронной структурой. У атомов металлов внутренние энергетические оболочки заполнены полностью, и наружная оболочка содержит всего несколько электронов. Это создает сильное взаимодействие электронов наружной оболочки с положительно заряженным ядром, которое слабо противостоит отдаче электронов, что делает их легко доступными для взаимодействия с другими атомами и молекулами.
Почему электроны в атомах металлов могут быть легко оторваны?
Отрыв электронов в атомах металлов возможен благодаря низкой энергии ионизации металлов. Энергия ионизации - это энергия, необходимая для отрыва одного электрона от атома. У атомов металлов эта энергия обычно находится на низком уровне, что связано с особенностями электронной структуры. Более конкретно, у атомов металлов внутренние энергетические оболочки заполнены полностью, и наружная оболочка содержит всего несколько электронов. Это создает сильное взаимодействие электронов наружной оболочки с положительно заряженным ядром и позволяет легко оторвать электроны от атома.
Какие факторы приводят к легкой отдаче электронов металлами?
Легкая отдача электронов металлами обусловлена несколькими факторами. Во-первых, у атомов металлов внутренние энергетические оболочки заполнены полностью, и наружная оболочка содержит всего несколько электронов. Это создает сильное взаимодействие электронов наружной оболочки с положительно заряженным ядром. Во-вторых, металлы обладают большим количеством свободных электронов, которые могут легко передвигаться внутри материала. Это обеспечивает возможность переноса электронов от одного атома к другому. И, наконец, металлы обладают высокой электропроводностью, что связано с легкой отдачей электронов и способностью электронов быстро двигаться в материале.