Взаимодействие металлов с водой может вызывать различные химические реакции, в результате которых образуются оксиды металлов. Оксиды — это соединения металлов с кислородом, которые могут быть как кислотными, так и основными. Реакция металла с водой может происходить с образованием оксида и выделением водорода или с образованием оксида и гидроксида металла.
Один из примеров металлов, образующих оксиды при взаимодействии с водой, — это щелочные металлы, такие как натрий и калий. Вода реагирует с ними, образуя гидроксиды соответствующих металлов и выделяя водород. Эта реакция является очень быстрой и сопровождается выделением большого количества тепла.
Еще одним примером металлов, образующих оксиды при взаимодействии с водой, являются щелочноземельные металлы, такие как кальций и магний. Они также реагируют с водой, образуя соответствующие гидроксиды и выделяя водород. Однако, в отличие от щелочных металлов, реакция с щелочноземельными металлами протекает медленнее и не так интенсивно.
Таким образом, взаимодействие металлов с водой может приводить к образованию оксидов, которые обладают как кислотными, так и основными свойствами. Эти реакции являются важными с точки зрения химии и имеют широкое применение в промышленности и научных исследованиях.
Оксидообразование металлов: особенности взаимодействия с водой

Взаимодействие металлов с водой является одним из основных способов образования оксидов. Оксиды обладают широким спектром свойств и широко используются в различных отраслях промышленности. Однако, каждый металл проявляет свою специфику в процессе взаимодействия с водой.
Некоторые металлы, такие как литий (Li), натрий (Na) и калий (K), проявляют сильное взаимодействие с водой. При контакте с водой они выделяются особенно активно, шипят и выделяются горючие газы. В результате взаимодействия этих металлов с водой образуются соответствующие оксиды и гидроксиды.
Другие металлы, такие как железо (Fe) и цинк (Zn), проявляют менее активное взаимодействие с водой. При взаимодействии этих металлов с водой образуются соответствующие гидроксиды. Например, железо вступает во взаимодействие с водой, образуя гидроксид Fe(OH)2 или Fe(OH)3, в зависимости от условий реакции.
Также существуют металлы, которые не вступают в прямое взаимодействие с водой, но могут образовывать оксиды при взаимодействии со взвешенными веществами, наличие которых приводит к низкому редокс-потенциалу. Например, алюминий (Al) образует оксид Al2O3 при взаимодействии с кислородом, который содержится в влаге.
Таким образом, каждый металл имеет свои особенности взаимодействия с водой и образования оксидов. Знание этих особенностей позволяет правильно выбирать металлы и контролировать процессы образования оксидов в различных сферах применения.
Щелочные металлы и их оксиды
Щелочные металлы - это группа элементов, которые расположены в первой группе периодической системы. В эту группу входят литий (Li), натрий (Na), калий (K), рубидий (Rb) и цезий (Cs). Щелочные металлы обладают химическими свойствами, схожими с щелочами.
Щелочные металлы образуют оксиды при взаимодействии с кислородом или водой. Одним из наиболее распространенных оксидов щелочных металлов является оксид лития (Li2O), который образуется при взаимодействии лития с кислородом. Этот оксид имеет сильные основные свойства.
Оксиды щелочных металлов также могут быть образованы при реакции металлов с водой. Например, натрий образует оксид натрия (Na2O) при реакции с водой. Этот оксид имеет свойства щелочи и способен образовывать гидроксид натрия (NaOH) при растворении в воде.
Оксиды щелочных металлов широко используются в разных отраслях промышленности. Например, оксид лития используется в производстве керамики и стекла, а оксид натрия является важным компонентом для производства стекла, щелочей и мыла.
Таким образом, оксиды щелочных металлов при взаимодействии с водой играют важную роль в различных химических процессах и обладают значительным промышленным значением. Они являются основными веществами и широко применяются в разных областях нашей жизни.
Щелочноземельные металлы и их оксиды
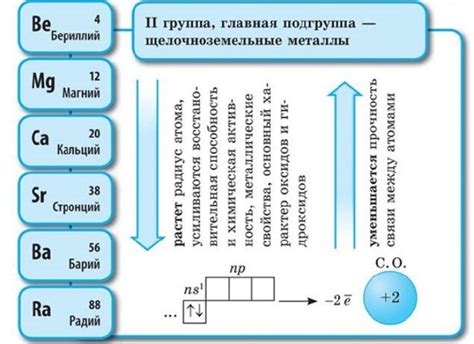
Щелочноземельные металлы – это группа элементов, которые находятся во второй группе периодической таблицы. Они включают бериллий, магний, кальций, стронций, барий и радий. Эти металлы характеризуются высокой реактивностью и являются важными элементами в различных областях промышленности и науки.
Оксиды щелочноземельных металлов образуются при взаимодействии металлов с кислородом воздуха или водой. Они обладают различными свойствами и находят применение в разных отраслях промышленности.
Бериллий образует оксид BeO, который известен своей высокой теплопроводностью и электроизоляционными свойствами. Это делает его полезным материалом в изготовлении электронных устройств и термоэлектрических материалов.
Магний образует оксид MgO, который является одним из наиболее распространенных оксидов магния. Он обладает высокой степенью жаропрочности и широко используется в производстве огнеупорных материалов, стекла и керамики.
Кальций образует оксид CaO, который известен как нормальный извести. Он широко используется в строительной и химической промышленности для производства цемента, стекла, огнетушителей и других продуктов.
Стронций образует оксид SrO, который используется в производстве красок, стекла и пигментов. Он также применяется в ядерных реакторах в качестве защитного покрытия для контроля радиоактивности.
Барий образует оксид BaO, который используется в производстве электронных устройств, стекла и керамики. Он также применяется в ядерной энергетике, медицине и других отраслях промышленности.
Радий образует оксид RaO, который имеет высокую радиоактивность и известен своим ядерным распадом. Он используется в научных исследованиях и в медицине для лечения рака.
Металлы переходного периода: образование оксидов при реакции с водой
Металлы переходного периода, такие как железо, медь, цинк, никель и др., проявляют свои характеристические свойства при взаимодействии с водой. В результате этой реакции образуются оксиды металлов.
Вода, взаимодействуя с металлами, обеспечивает окисление металла и превращение его в соответствующий оксид. Так, при взаимодействии железа с водой образуется оксид железа (III) - Fe2O3, при взаимодействии меди - оксид меди (II) - CuO, при взаимодействии цинка - оксид цинка (II) - ZnO и т.д.
Образование оксидов при взаимодействии с водой имеет важное практическое применение. Например, оксиды металлов широко используются в промышленности для получения красителей, лакокрасочных материалов и катализаторов. Кроме того, оксиды переходных металлов играют ключевую роль в электрохимических процессах, таких как электролиз и гальваническая коррозия.
В обобщенном виде реакция взаимодействия металлов переходного периода с водой может быть представлена следующим образом:
| Металл | Оксид, образующийся при реакции с водой |
|---|---|
| Железо | Fe2O3 |
| Медь | CuO |
| Цинк | ZnO |
| Никель | NiO |
| Кобальт | CoO |
Таким образом, металлы переходного периода образуют оксиды при реакции с водой, что находит свое применение в различных отраслях промышленности и электрохимии.
Оксидообразование алюминия и его влияние на воду

Алюминий является одним из металлов, образующих оксиды при взаимодействии с водой. В результате окислительного взаимодействия алюминия с водой образуется оксид алюминия (Al2O3), который по своей структуре представляет собой кристаллическую сеть.
Окислительные свойства алюминия могут быть использованы в различных областях. Например, оксид алюминия служит важным компонентом в процессе анодирования алюминиевых поверхностей, позволяя повысить их стойкость к коррозии и износу.
Однако, при контакте с водой оксид алюминия может оказывать определенное влияние на химический состав и свойства воды. В частности, оксид алюминия способен адсорбировать на свою поверхность различные ионы, в том числе и ионы металлов, что может приводить к изменению качества воды.
Использование алюминиевых соединений, содержащих оксид алюминия, в процессе очистки воды позволяет удалить из нее различные загрязнения, такие как органические вещества, токсичные металлы и пестициды. Оксид алюминия действует как коагулянт, помогая собрать и сконденсировать мельчайшие частицы, образуя твердое вещество, которое удобно отделять от воды.
Тяжелые металлы и оксиды: взаимодействие с водой и его последствия
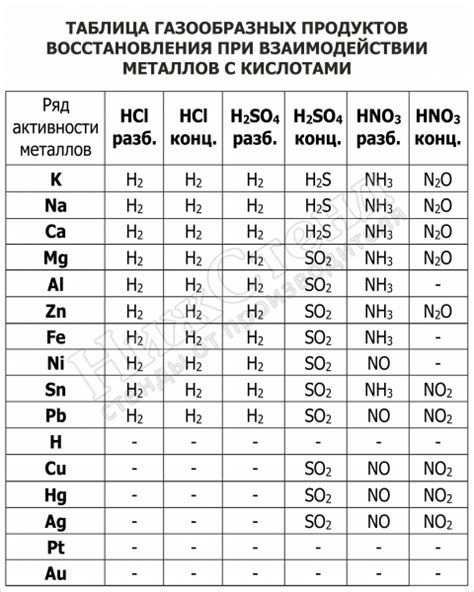
Тяжелые металлы, такие как свинец, ртуть и кадмий, могут образовывать оксиды при взаимодействии с водой. Оксиды данных металлов обладают различными свойствами и могут оказывать разнообразное влияние на окружающую среду.
Взаимодействие тяжелых металлов с водой приводит к образованию оксидов, которые в свою очередь могут переходить в растворимые формы. Это может привести к проблемам экологического характера, так как растворимые соединения тяжелых металлов имеют токсические свойства и могут накапливаться в почве и воде.
Кроме того, некоторые оксиды тяжелых металлов могут вызывать кислотификацию водных систем. Они реагируют с водой и образуют кислоту, что изменяет рН водной среды и может привести к гибели растений и животных, а также к разрушению экосистем.
Оксиды тяжелых металлов также могут накапливаться в организмах живых существ, вызывая различные заболевания. К примеру, свинец, образуя оксиды, может накапливаться в почках и вызывать их недостаточность, а ртуть может накапливаться в мозге и приводить к нарушениям нервной системы.
Все это позволяет сделать вывод о том, что взаимодействие тяжелых металлов с водой и образование оксидов имеет серьезные последствия для окружающей среды и здоровья людей. Поэтому важно контролировать выбросы таких металлов и находить пути по их очистке из водных систем и почвы.
Полуфабрикаты и легирование металлов: важные факторы оксидообразования
В процессе производства металлов и их сплавов, важную роль играют полуфабрикаты, которые являются промежуточным этапом между первичной рудой и готовым металлическим изделием.
Оксидообразование при взаимодействии металлов с водой является непрерывным процессом, который может влиять на качество и свойства металлических изделий. Важные факторы, которые влияют на оксидообразование, включают химический состав металла, его структуру, температуру окружающей среды и время взаимодействия.
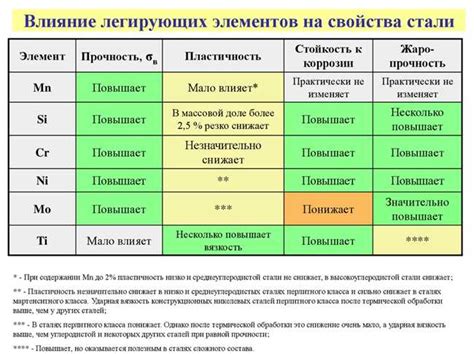
Легирование металлов, то есть введение специальных примесей, также может оказывать значительное влияние на оксидообразование. Добавление определенных элементов может способствовать устойчивому образованию защитной пленки оксида на поверхности металла, что улучшает его коррозионную стойкость.
Специальные примеси, такие как хром, алюминий или цинк, могут создавать защитные оксидные слои, которые предотвращают доступ кислорода и влаги к металлической поверхности. Это может быть особенно важно для металлов, которые сами по себе склонны к оксиdации и коррозии, таких как железо или алюминий.
Таким образом, полуфабрикаты и процесс легирования металлов являются важными факторами, которые нужно учитывать при производстве металлических изделий. Они позволяют контролировать оксидообразование и повышать стойкость металла к коррозии, что влияет на его долговечность и надежность.
Роль оксидов металлов в промышленных процессах и экологическая проблематика
Оксиды металлов играют важную роль в промышленных процессах, являясь основными компонентами различных материалов, используемых в разных областях промышленности. Они обладают разнообразными свойствами, такими как высокая термическая и электрическая проводимость, высокая прочность и химическая стойкость.
Однако, взаимодействие оксидов металлов с водой может иметь негативные экологические последствия. При контакте с водой некоторые оксиды металлов могут образовывать кислоты или щелочи, которые могут загрязнять природные водоемы или негативно повлиять на качество питьевой воды.
Например, оксиды серы при взаимодействии с водой образуют серную кислоту, которая является сильным коррозионным веществом и может привести к загрязнению окружающей среды и угрозе здоровью человека. Помимо этого, оксиды железа, алюминия и других металлов также могут вызывать изменение pH воды, что может негативно сказаться на биологическом разнообразии водных экосистем.
Экологическая проблематика, связанная с взаимодействием оксидов металлов с водой, требует внимания и разработки специальных методов обработки и очистки сточных вод, а также контроля и регулирования выбросов оксидов металлов в окружающую среду. Важно принимать меры для снижения загрязнения водных ресурсов и сохранения экологического равновесия.
Способы контроля оксидообразования металлов при взаимодействии с водой
Металлы, образующие оксиды при взаимодействии с водой, могут быть подвержены различным реакциям, которые влияют на их поведение и свойства. Одним из способов контроля оксидообразования металлов является регулирование условий их взаимодействия с водой.
Один из способов контроля оксидообразования металлов - это поддержание определенной температуры воды, с которой они взаимодействуют. Высокая температура может увеличить скорость оксидообразования, тогда как низкая температура может замедлить или полностью предотвратить его.
Другим способом контроля оксидообразования металлов является добавление ингибиторов или антиоксидантов, которые могут замедлить или полностью предотвратить процесс оксидации при взаимодействии металлов с водой. Ингибиторы могут быть добавлены в виде растворов или покрытий на поверхности металла.
Также возможен контроль оксидообразования металлов путем изменения их поверхности. Например, поверхность металла может быть покрыта специальными пленками или обработана специальными методами, которые могут изменить процесс оксидообразования или предотвратить его полностью.
Важно отметить, что способы контроля оксидообразования металлов при взаимодействии с водой могут различаться в зависимости от конкретного металла и условий взаимодействия. Поэтому выбор оптимального способа контроля требует проведения исследований и анализа конкретных условий использования металла.
Вопрос-ответ
Какие металлы образуют оксиды при взаимодействии с водой?
Некоторые металлы, такие как натрий, калий, кальций и магний, образуют оксиды при взаимодействии с водой.
Какие оксиды образуются при взаимодействии металлов с водой?
Металлы, такие как натрий и калий, образуют гидроксиды и основания при реакции с водой. Например, натрий образует гидроксид натрия (NaOH), а калий - гидроксид калия (KOH). Кальций и магний также образуют гидроксиды и основания.
Что происходит при взаимодействии натрия с водой?
В результате взаимодействия натрия с водой образуется гидроксид натрия (NaOH) и обильное выделение водорода. Эта реакция является самой быстрой и очень экзотермической, то есть сопровождается выделением большого количества тепла.
Каковы особенности взаимодействия калия с водой?
При контакте калия с водой происходит быстрая реакция, при которой образуется гидроксид калия (KOH) и выделяется водород. Взаимодействие калия с водой также сопровождается сильным выделением тепла.
Что происходит при контакте кальция с водой?
Кальций при взаимодействии с водой образует гидроксид кальция (Ca(OH)2) и выделяется водород. Реакция происходит умеренно быстро и сопровождается выделением тепла, но не таким сильным, как при взаимодействии натрия или калия.
Каковы результаты взаимодействия магния с водой?
При реакции магния с водой образуется гидроксид магния (Mg(OH)2) и выделяется водород. Эта реакция происходит медленно и требует больше времени, чем реакции с натрием, калием или кальцием. Также выделение тепла при этой реакции не такое интенсивное.
Какие свойства имеют образовавшиеся гидроксиды и основания при реакции металлов с водой?
Гидроксиды и основания, образующиеся при реакции металлов с водой, обладают щелочными свойствами. Они растворяются в воде и продуцируют ионы гидроксида (OH-) , что делает раствор щелочным. Гидроксиды и основания используются в различных отраслях промышленности и в быту.

