В химии существует множество металлов, способных реагировать с кислородом. Однако не все они проявляют одинаковую энергичность в этом процессе. Среди всех металлов наиболее энергично реагируют щелочные металлы, такие как литий (Li), натрий (Na), калий (K) и рубидий (Rb).
Эти металлы характеризуются низкой ионизационной энергией, что позволяет им очень легко отдавать электроны и образовывать ионы положительного заряда. При взаимодействии с кислородом, они образуют металлические оксиды, которые проявляют сильные основные свойства.
Например, литий, реагируя с кислородом, образует литиевый оксид (Li2O), который обладает амфотерными свойствами. Это значит, что он может как растворяться в кислых растворах, образуя соли лития, так и растворяться в щелочных растворах, образуя гидроксид лития. В результате реакции с кислородом щелочные металлы проявляют свою высокую реакционность и способность образовывать различные соединения.
Основные факты

Металлы - это широкий класс элементов, которые характеризуются высокой электропроводностью, благодаря свободным электронам в их структуре. Многие металлы реагируют с кислородом при нагревании или контакте, образуя оксиды.
Однако, наиболее энергично с кислородом реагируют щелочные металлы, такие как литий (Li), натрий (Na), калий (K) и рубидий (Rb). Они обладают высокой реактивностью и могут гореть при контакте с воздухом или водой.
Это происходит из-за того, что металлы щелочных металлов имеют одну электронную оболочку, которая легко потеряется при контакте с кислородом. Это позволяет металлам быстро окисляться, образуя соединения с кислородом.
Таким образом, щелочные металлы реагируют с кислородом наиболее энергично из всех металлов. Их реакция с кислородом особенно заметна при взаимодействии с водой, когда металлы начинают интенсивно гореть и выделяться водород.
Какой металл наиболее активно реагирует с кислородом?
Среди всех металлов наиболее активно с кислородом реагируют щелочные металлы - литий (Li), натрий (Na), калий (K), рубидий (Rb) и цезий (Cs). Эти металлы представляют первую группу периодической системы элементов и сильно реагируют с кислородом из-за своей высокой электроотрицательности.
При контакте с кислородом щелочные металлы образуют оксиды, которые обладают высокой степенью ионизирования. Окисление металла в оксиде происходит за счет передачи электронов от металла к кислороду. Реакция резко протекает с выделением тепла и образованием огненного пламени. Кроме того, при реакции с кислородом щелочные металлы могут выделять водород.
В химических реакциях с кислородом щелочные металлы проявляют свою высокую активность и реактивность. Они используются в промышленности для получения различных оксидов и перекисей, а также в химическом анализе и синтезе органических соединений.
Причины энергичной реакции с кислородом
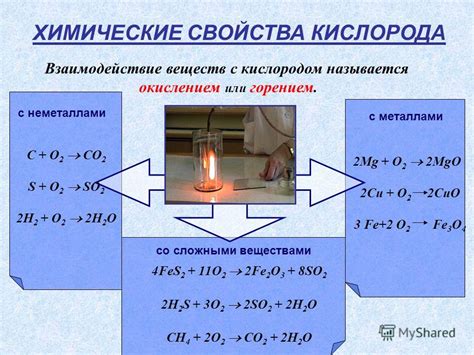
Реакция металлов с кислородом - это процесс, при котором металлы окисляются, а кислород - восстанавливается. Некоторые металлы реагируют с кислородом настолько энергично, что образуют пламя или даже могут взорваться. Это связано с несколькими причинами.
Во-первых, металлы имеют низкую энергию ионизации, что позволяет им быстро отдавать электроны в реакции с кислородом. Такие металлы, как литий, натрий и калий, обладают особенно низкой энергией ионизации, поэтому реакция с кислородом у них происходит очень быстро и энергично.
Во-вторых, металлы образуют оксиды с кислородом, которые являются стабильными соединениями. Однако, некоторые металлические окислы, например пероксиды и супероксиды, обладают очень высокой реакционной способностью и могут реагировать с кислородом еще более энергично.
Кроме того, металлы могут быть очень реакционноспособными из-за своей кристаллической структуры. Некоторые металлы образуют атомарные или молекулярные формы при нагреве, что позволяет им проникать внутрь молекул кислорода и менять его структуру.
Также стоит отметить, что реакция металлов с кислородом усиливается в условиях повышенной температуры или наличия катализаторов. Это связано с тем, что повышенная температура или катализаторы могут активировать поверхность металла и ускорить реакцию.
Реакция с кислородом
Реакция металлов с кислородом - это процесс, при котором металлы вступают в химическую реакцию с кислородом из воздуха. Некоторые металлы реагируют с кислородом настолько энергично, что при этом возникает яркий световой эффект и выделяется большое количество тепла. Это явление называется горением металлов.
Наиболее энергично с кислородом реагируют щелочные металлы, такие как литий (Li), натрий (Na) и калий (K). При контакте с кислородом, эти металлы быстро окисляются и выделяют яркий пламя. Например, при сжигании кусочка лития можно наблюдать ярко-красное пламя.
Однако реакция с кислородом не всегда является желательной. Некоторые металлы, такие как железо (Fe) и алюминий (Al), также реагируют с кислородом, но при этом образуют покрытие оксидов, которое защищает их от дальнейшей коррозии. Это свойство делает данные металлы более устойчивыми к окислению и образованию ржавчины.
Реакция с кислородом важна не только с точки зрения химии, но и в промышленных и бытовых целях. Например, при производстве стали, реакция железа с кислородом играет ключевую роль в процессе образования сплавов и придания металлу необходимых свойств. Кроме того, металлические элементы, которые образуют оксиды при реакции с кислородом, часто используются в качестве красителей для окраски стекла или керамики.
Примеры химических реакций
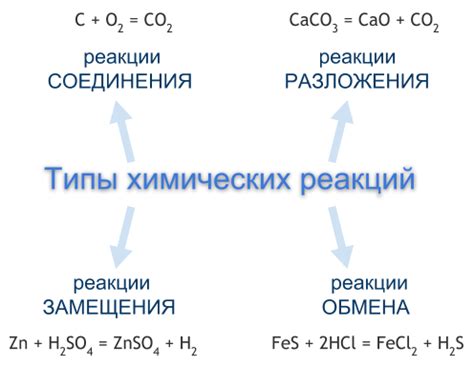
Химические реакции – это процессы, при которых происходит превращение веществ в другие вещества с образованием новых связей. Некоторые из них проходят с особой энергией и способны вызвать взрывы или сильные пожары. Одним из примеров таких реакций является реакция металла с кислородом.
Наиболее энергично с кислородом реагирует металл натрий. При взаимодействии натрия с кислородом образуется оксид натрия (Na2O), который обладает высокой химической активностью. Реакция протекает с выделением большого количества тепла и света. В результате образуется горящий металлический шарик, который стремительно двигается по воздуху.
Еще одним примером химической реакции с высокой энергетикой является горение алюминия. При реакции алюминия с кислородом образуется оксид алюминия (Al2O3), который является структурным компонентом глины и керамики. Реакция протекает с высвобождением большого количества тепла и света, и алюминий можно использовать в качестве топлива для закрепления взрывчатых веществ.
Также стоит отметить реакцию магния с кислородом. При нагревании магния и последующем его контакте с кислородом образуется оксид магния (MgO). Реакция сопровождается выделением яркого света и обладает высокой тепловой энергией. Магний с горением протекает очень быстро и может быть использован в ракетных или фейерверковых смесях.
Реакция с кислородной группой
Кислород - одно из самых распространенных элементов на Земле, который активно взаимодействует с различными веществами. Наиболее энергичной реакцией с кислородом обладают активные металлы.
В таблице химических элементов можно найти несколько металлов, способных сильно реагировать с кислородом. В первую очередь стоит отметить литий (Li), который образует горящую яркую пламя при взаимодействии с воздухом. Эта реакция идет с выделением большого количества энергии.
Также в эту группу металлов входит натрий (Na), который также прекрасно реагирует с кислородом. При контакте с воздухом натрий плавится и образует ослепительно яркий огонь. Эта реакция также сопровождается выделением большого количества тепла.
Отдельно стоит упомянуть калий (K), который проявляет сходные свойства с литием и натрием. Реакция калия с кислородом воздуха происходит с большим пылевыделением и образованием белой пыли. Такой вид реакции с кислородом может привести к возгоранию калия.
Итак, на основании данных по химически активным металлам, можно сделать вывод, что литий, натрий и калий проявляют наиболее энергичную реакцию с кислородом, при этом выделяя большое количество энергии и создавая яркий огонь или пламя.
Свойства и применение

Металлы, способные реагировать с кислородом наиболее энергично, обладают рядом уникальных свойств, которые находят широкое применение в различных отраслях промышленности и научных исследованиях.
Одним из таких металлов является прочный и коррозионностойкий алюминий. Этот металл образует на поверхности оксидную пленку, что делает его устойчивым к процессам окисления. Благодаря этим свойствам, алюминий используется в производстве авиационной и космической техники, а также в строительстве и электротехнике.
Еще одним металлом, отличающимся высокой энергичностью реакции с кислородом, является титан. Титановые сплавы обладают высокой прочностью и легкостью, поэтому широко используются в авиационной, автомобильной и медицинской промышленности.
Другим металлом, реагирующим с кислородом активно, является магний. Магниевые сплавы обладают низкой плотностью и хорошей устойчивостью к коррозии, что делает их идеальными для использования в составе автомобильных деталей, а также в производстве легких конструкций, например, в аэрокосмической отрасли.
Оксиды металлов, получаемые при реакции с кислородом, также имеют широкие применения. Например, оксид железа (Fe2O3) используется в производстве красок и косметики, оксид цинка (ZnO) применяется в лекарственной промышленности и производстве стекол, а оксид алюминия (Al2O3) является основным компонентом керамики и полупроводниковой промышленности.
Вопрос-ответ
Какой металл реагирует с кислородом наиболее энергично?
Наиболее энергично с кислородом реагирует металл литий (Li).
Какой металл обладает наибольшей склонностью к реакции с кислородом?
Металл литий (Li) обладает наибольшей склонностью к реакции с кислородом.
Какой металл реагирует наиболее активно с кислородом?
Металл литий (Li) реагирует наиболее активно с кислородом.
Какой металл образует наиболее энергичные соединения с кислородом?
Металл литий (Li) образует наиболее энергичные соединения с кислородом.
