Последний энергетический уровень металлов — особый параметр, определяющий их химические и физические свойства. Данный уровень является наиболее удаленным от ядра и содержит наибольшее количество электронов среди всех энергетических уровней атома. Количество электронов на последнем энергетическом уровне, а также способность этих электронов вступать в химические реакции имеют решающее значение для свойств и поведения металлов.
Более специфично, количество электронов на последнем энергетическом уровне, также известном как валентность, определяет, насколько металл способен образовывать химические связи с другими элементами. Металлы с полностью заполненным последним энергетическим уровнем имеют наименьшую валентность и, как следствие, не образуют химические связи с другими атомами легко. В свою очередь, металлы с неполностью заполненным последним энергетическим уровнем обладают высокой валентностью и проявляют большую склонность к образованию химических соединений.
Количество электронов на последнем энергетическом уровне оказывает влияние на множество свойств металлов. Важно отметить, что металлы с полностью заполненным последним энергетическим уровнем, например, инертные газы, обладают высокой термической и электрической проводимостью. С другой стороны, металлы с неполностью заполненным последним энергетическим уровнем имеют свойства, такие как деформация, пластичность, устойчивость к коррозии.
Особенности энергетического уровня металлов

Металлы являются одним из основных классов химических элементов. Их особенностью является наличие свободных электронов на последнем энергетическом уровне. Это делает металлы хорошими проводниками электричества и тепла.
Большинство металлов имеют на последнем энергетическом уровне 1-3 электрона. Исключение составляют металлы переходных элементов, которые имеют на последнем энергетическом уровне от 1 до 12 электронов.
Наличие свободных электронов на последнем энергетическом уровне у металлов влияет на их физические и химические свойства. Относительно низкая энергия их проводимости и высокая подвижность электронов делает металлы хорошими проводниками электричества.
Также свободные электроны в металлах способствуют высокой теплопроводности. Они обладают большой скоростью движения и передают тепло другим электронам и ионам в материале, что обеспечивает эффективную передачу тепла.
Особенности энергетического уровня металлов связаны с их способностью образовывать ионные соединения. Металлы имеют тенденцию отдавать свои свободные электроны и образовывать положительно заряженные ионы, которые притягиваются к отрицательно заряженным атомам или молекулам.
Металлы и их строение атомов
Металлы обладают особым строением атомов, которое отличает их от других элементов. Атом металла состоит из центрального ядра и облака электронов, которые образуют электронную оболочку.
Центральное ядро атома металла содержит протоны и нейтроны. Протоны имеют положительный заряд, а нейтроны не имеют заряда вообще. Общее количество протонов и нейтронов в ядре определяет атомную массу металла.
Электронная оболочка атома металла состоит из электронов, которые движутся вокруг ядра по определенным орбитам. Электроны имеют отрицательный заряд и служат для формирования химических связей между атомами металла.
На последнем энергетическом уровне атома металла находится некоторое количество электронов. Именно это количество электронов на последней оболочке определяет химические свойства металла и его способность образовывать ионные связи с другими элементами.
Обычно, у металлов количество электронов на последней оболочке меньше полного значения, что делает металлы склонными отдавать электроны и образовывать положительно заряженные ионы. Именно это свойство обуславливает хорошую электропроводимость и теплопроводность металлов.
Энергетические уровни и электронная конфигурация
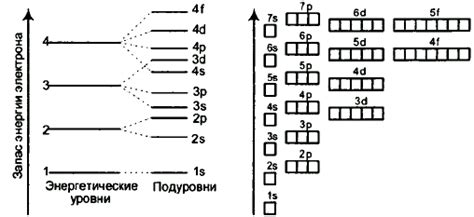
Количество электронов на последнем энергетическом уровне у металлов определяет их свойства и особенности. Энергетические уровни - это уровни энергии, на которых находятся электроны в атоме металла. Каждый электрон занимает определенную энергетическую область и имеет свою электронную конфигурацию.
Электронная конфигурация - это представление расположения электронов по энергетическим уровням и подуровням в атоме. Она характеризуется последовательностью чисел и букв, описывающих количество электронов на каждом уровне и подуровне. На последнем энергетическом уровне находятся валентные электроны, которые обуславливают химические свойства металла.
Металлы обычно имеют малое количество электронов на последнем энергетическом уровне. Это связано с их положением в периодической системе элементов и особенностями заполнения электронных оболочек. Например, металлы в колонке 1 периодической системы имеют один валентный электрон на последнем энергетическом уровне, что делает их хорошими проводниками электричества и тепла.
Некоторые металлы имеют большее количество электронов на последнем энергетическом уровне, что влияет на их свойства. Например, металлы в колонке 14 периодической системы имеют четыре валентных электрона на последнем энергетическом уровне, что делает их химически активными и способными образовывать соединения с другими элементами.
Количество электронов на последнем энергетическом уровне у металлов
Металлы – это класс элементов, характеризующихся способностью отдавать электроны и образовывать положительно заряженные ионы. Количество электронов на последнем энергетическом уровне у металлов имеет свои особенности.
Большинство металлов имеют один-два электрона на последнем энергетическом уровне. Это позволяет им легко отдавать эти электроны и образовывать двухвалентные или однозарядные ионы. Например, натрий (Na) имеет один электрон на последнем энергетическом уровне и, отдав его, образует положительный ион Na+.
Однако, существуют металлы, у которых на последнем энергетическом уровне может быть более двух электронов. Например, железо (Fe) имеет два электрона на последнем энергетическом уровне и, в результате, может образовывать разноименные ионы, такие как Fe2+ и Fe3+.
Исключением из правила являются транзиционные металлы, у которых количество электронов на последнем энергетическом уровне не всегда одинаково. Например, медь (Cu) и цинк (Zn) имеют одно электрон на последнем энергетическом уровне, однако медь может образовывать разноименные ионы Cu+ и Cu2+, а цинк всегда образует двухвалентный ион Zn2+.
Таким образом, количество электронов на последнем энергетическом уровне у металлов может быть разным и определяет их способность образовывать ионы и участвовать в химических реакциях.
Влияние количества электронов на свойства металлов
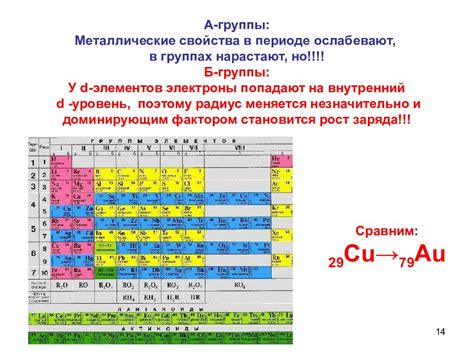
Металлы являются одним из основных типов химических элементов. Одной из особенностей металлов является их способность образовывать положительно заряженные ионы, основанную на потере электронов с последнего энергетического уровня. Количество электронов на последнем энергетическом уровне у металлов влияет на их химические и физические свойства.
Чем меньше количество электронов на последнем энергетическом уровне у металла, тем он более активен и склонен к химическим реакциям. Например, щелочные металлы, такие как литий и натрий, имеют только один электрон на последнем энергетическом уровне и легко реагируют с водой и кислородом. Это делает их очень реактивными и опасными при обращении с ними.
С другой стороны, металлы с большим количеством электронов на последнем энергетическом уровне обладают более слабыми химическими свойствами и менее склонны к реакциям. Например, железо и серебро имеют относительно большое количество электронов на последнем энергетическом уровне и обычно проявляют меньшую реактивность, чем щелочные металлы.
Количество электронов на последнем энергетическом уровне также влияет на физические свойства металлов, такие как плавление и кипение. Металлы с более низким количеством электронов на последнем энергетическом уровне обычно имеют более низкую температуру плавления и кипения, что делает их более подходящими для использования в различных промышленных процессах.
Таким образом, количество электронов на последнем энергетическом уровне является важным фактором, определяющим химические и физические свойства металлов. Это позволяет нам лучше понять и использовать эти материалы в различных областях науки и промышленности.
Вопрос-ответ
Какие металлы имеют наибольшее количество электронов на последнем энергетическом уровне?
Наибольшее количество электронов на последнем энергетическом уровне имеют металлы из переходных и благородных серий периодической таблицы, такие как железо (Fe) и золото (Au).
Какое значение имеет количество электронов на последнем энергетическом уровне для свойств металлов?
Количество электронов на последнем энергетическом уровне влияет на химические и физические свойства металлов. Оно определяет их способность к образованию связей с другими атомами и их реактивность. Чем меньше электронов на последнем уровне, тем больше металл будет склонен к образованию положительных ионов и тем большую теплопроводность и электропроводность он будет обладать.
Какова особенность электронной конфигурации металлов?
Особенностью металлов является то, что у них на последнем энергетическом уровне находятся от одного до трех электронов. Это связано с особенностями расположения металлов в периодической таблице и их электронной конфигурацией.
Может ли количество электронов на последнем энергетическом уровне варьироваться у металлов?
Да, количество электронов на последнем энергетическом уровне может варьироваться у металлов. Например, у калия (K) есть один электрон на последнем уровне, а у кальция (Ca) и алюминия (Al) уже два электрона. Это зависит от их положения в периодической таблице и электронной конфигурации.
Как наличие электронов на последнем энергетическом уровне влияет на свойства металлов?
Наличие электронов на последнем энергетическом уровне влияет на свойства металлов. Они облегчают образование химических связей с другими атомами, что позволяет металлам образовывать соединения и сплавы. Электроны на последнем уровне также обеспечивают металлам их характерные физические свойства, такие как теплопроводность и электропроводность.

