Атомы - основные строительные элементы вещества, которые состоят из электронов, протонов и нейтронов. Каждый атом имеет определенную электронную конфигурацию, которая определяет его свойства и активность.
Наиболее активным металлом считается франций (Fr), который находится в самой нижней группе периодической системы элементов. Франций является последним элементом в группе щелочных металлов, и его атом имеет 87 электронов.
Электронная конфигурация атома франция может быть представлена как: 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 6s1 7s1. Внешний электронный слой франция состоит из одного электрона в s-орбитале, что делает его очень реактивным.
Из-за своей высокой активности, франций является очень редким и опасным элементом. Его использование в научных и промышленных целях крайне ограничено из-за его высокой воспламеняемости и радиоактивных свойств. Однако исследования атома франция помогают ученым лучше понять структуру и свойства атомов и молекул в общем.
Электронная конфигурация атома франция подтверждает его невероятную реактивность и способность образовывать ионы с положительным зарядом, которые легко реагируют с другими элементами и молекулами. Эти свойства франция подтверждают исключительную химическую активность самого активного металла в периодической системе элементов.
Электронная конфигурация
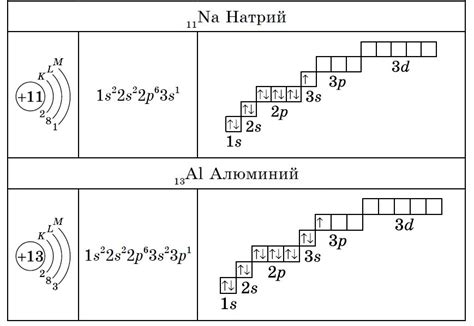
Электронная конфигурация атома наиболее активного металла, обычно представляет собой последовательность заполнения энергетических уровней электронами. Для определения электронной конфигурации активного металла, необходимо знать его атомный номер и распределение электронов по энергетическим уровням.
Наиболее активным металлом в таблице Менделеева является франций (Fr), который имеет атомный номер 87. В его атоме располагается 87 электронов. Полная электронная конфигурация франция можно записать следующим образом:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s1
Атом франция имеет 7 энергетических уровней, на которых расположены электроны. На первом уровне находятся 2 электрона, на втором - 8, на третьем - 18. Четвертый уровень содержит 32 электрона, пятый - 18, шестой - 32 и на седьмом находится только 1 электрон, что делает этот металл очень активным.
Электронная конфигурация определяет химические свойства металла, такие как его реакционную способность, способность образовывать соединения и реагировать с другими веществами. Франций, являясь самым активным металлом, обладает высокой реакционной способностью и быстро вступает в химические реакции с веществами в своем окружении.
Активный металл
Активный металл – это металл, обладающий высокой химической активностью и способностью вступать в реакцию с другими веществами, особенно с кислородом или водой.
Наиболее активным металлом в периодической системе элементов является франций, принадлежащий к группе щелочных металлов. Его атом имеет электронную конфигурацию 2-8-18-32-18-8-1.
Активность металла обусловлена его способностью легко отдавать электроны и образовывать ионы положительного заряда. Именно благодаря этим свойствам активные металлы реактивны и способны вызывать сильные химические реакции.
Активные металлы активно реагируют с кислородом из воздуха, приводя к образованию оксидов металла. Например, натрий реагирует с кислородом и образует оксид натрия (Na2O).
Многие активные металлы также быстро вступают в реакцию с водой, образуя гидроксиды и высвобождая водород. Например, реакция натрия с водой приводит к образованию гидроксида натрия (NaOH) и выделению водорода (H2)
Активные металлы широко используются в промышленности, в том числе в процессах производства сплавов, цветных металлов, электродов и других материалов. Они также могут использоваться в различных химических реакциях и процессах.
Наиболее активный металл

Наиболее активный металл – это металл, обладающий высокой химической активностью по сравнению с другими металлами. Он способен легко вступать в реакции с другими веществами и обладает высокой реакционной способностью. Такой металл является хорошим окислителем и обычно имеет низкие значения энергии ионизации и электроотрицательности.
Наиболее активным металлом известным на данный момент является франций (Fr). Он принадлежит к группе алкалийных металлов и стоит в самом низу периодической системы, что объясняет его высокую активность. Франций представлен элементарным видом и обладает очень коротким сроком жизни из-за своей нестабильности. Он также является радиоактивным, что делает его использование в практических целях невозможным.
Электронная конфигурация атома франция можно записать следующим образом: 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^10 4p^6 5s^2 4d^10 5p^6 6s^1. В последней энергетической оболочке у атома франция находится всего один электрон, что делает его легким окислителем и очень активным элементом.
Благодаря своей активности, франций обладает различными применениями. Например, он может быть использован в исследованиях ядерной физики или в качестве источника частиц для различных экспериментов. В связи с его радиоактивностью, франция не имеет практического применения в обычном быту или в промышленности.
Хотя франций является наиболее активным металлом, не стоит забывать о его ограниченной доступности и опасности использования. Его изучение и эксперименты с ним должны проводиться под строгим контролем и соблюдением всех соответствующих мер безопасности.
Вопрос-ответ
Какая электронная конфигурация у атома наиболее активного металла?
Атом наиболее активного металла имеет электронную конфигурацию [эдив=1s^2, 2s^2, 2p^6, 3s^1].
Почему атом наиболее активного металла имеет такую электронную конфигурацию?
Атом наиболее активного металла имеет один электрон в валентной оболочке, что делает его нестабильным и стремящимся осуществить обмен этим электроном, чтобы достичь более стабильной конфигурации.
Какая периодическая таблица элементов содержит информацию о наиболее активном металле?
Информацию о наиболее активном металле можно найти в таблице D в периодической таблице элементов.
Какое место занимает наиболее активный металл в периодической таблице элементов?
Наиболее активный металл занимает первое место в первой группе периодической таблице элементов.
Какие свойства обуславливают активность наиболее активного металла?
Активность наиболее активного металла обуславливается его способностью переходить электрон во внешней оболочке на другие атомы, образуя положительные ионы.
Какие элементы имеют похожую электронную конфигурацию на атом наиболее активного металла?
Элементы, имеющие похожую электронную конфигурацию на атом наиболее активного металла, включают литий, натрий и калий, которые также имеют один электрон в валентной оболочке.