Температура плавления металлов является одним из важных параметров, определяющих их физические свойства. От лития до цезия температура плавления металлов постепенно изменяется, отражая особенности их строения и химического состава. Различия в температурах плавления металлов обусловлены различиями в межатомных связях, кристаллической структуре и взаимодействии атомов.
Литий - самый лёгкий металл в периодической системе, и его температура плавления составляет всего 180 градусов Цельсия. Это связано с тем, что у лития малое количество электронов в внешней оболочке, что облегчает нарушение кристаллической структуры и переход в жидкую фазу при низкой температуре.
Следующий элемент в периодической системе - натрий. У него температура плавления уже значительно выше и составляет 98 градусов Цельсия. Натрий имеет большее количество электронов в внешней оболочке, что осложняет нарушение кристаллической структуры и приводит к повышению температуры плавления.
Следующие элементы - калий, рубидий и цезий - имеют еще более высокую температуру плавления, которая составляет соответственно 64, 39 и 28 градусов Цельсия. Подобно натрию, у них также большое количество электронов во внешней оболочке, что усложняет нарушение кристаллической структуры, а значит, и переход в жидкую фазу.
Литий

Литий - металл, химический элемент из группы щелочных металлов. В периодической таблице литий имеет атомный номер 3 и обозначение Li. Он является наименее плотным металлом и обладает низкой температурой плавления.
Температура плавления лития составляет примерно 180 градусов Цельсия. Это довольно низкая температура по сравнению с другими металлами, такими как алюминий или железо. Благодаря этому литий можно легко плавить и формировать в различные изделия.
Литий обладает высокой электропроводностью и низкой плотностью, что делает его идеальным материалом для использования в аккумуляторах. Батареи, основанные на литиевых ионных технологиях, имеют высокую энергетическую плотность и длительное время работы.
Уникальные свойства лития позволяют его использование и в других областях. Например, литиевые сплавы применяются в авиационной и космической промышленности, так как они обладают низкой плотностью и высокой прочностью. Литий также используется в производстве лекарств и в сфере ядерной энергетики.
По своей природе литий является реактивным металлом и может очень быстро реагировать с водой или кислородом. В чистом виде литий является мягким и легким металлом, который может быть рассечен ножом или даже руками. Из-за своей реактивности литий обычно хранят в специальных контейнерах с протекцией от воздуха и влаги.
Натрий
Натрий – это металлический химический элемент с атомным номером 11, относящийся к щелочным металлам. Он обладает серебристо-белым металлическим блеском и является мягким и легким металлом. Натрий имеет атомную массу приблизительно равную 23 г/моль.
Температура плавления натрия составляет около 98 градусов Цельсия. Это означает, что натрий плавится при относительно низкой температуре. При этой температуре натрий переходит из твердого состояния в жидкое состояние. Плавление – это процесс, при котором твердое вещество превращается в жидкость под воздействием повышения температуры.
Как и другие щелочные металлы, натрий обладает низкой температурой плавления. Это объясняется тем, что атомы щелочных металлов имеют слабое взаимодействие между собой и образуют слабые связи, что делает их более подвижными и позволяет им легко переходить из твердого состояния в жидкое.
Калий

Калий (K) - химический элемент периодической системы, относится к щелочным металлам. Он имеет атомный номер 19 и обозначается символом K. Калий относится к блоку s, группе 1 и периоду 4.
Калий является серебряно-белым металлом, который становится мягким и легко резко под действием воздуха, которая влажная, реагировать с водой и даже горячей водой. Он легко окисляется и реагирует с кислородом, образуя оксид калия.
Температура плавления калия составляет около 63,5 градуса Цельсия, что делает его одним из низкоплавких щелочных металлов. Калий используется во многих промышленных процессах, включая производство удобрений, стекла, мыла и легких сплавов. Также калий является важным элементом в органической химии и биологии, где он играет важную роль в регуляции обмена веществ и функции клеток.
На периодической системе элементов калий расположен после натрия и магния, с которыми он имеет множество химических свойств. Некоторые из наиболее известных соединений калия включают хлорид калия (KCl), карбонат калия (K2CO3) и фосфат калия (KH2PO4). Они используются в различных отраслях промышленности и научных исследованиях.
Рубидий
Рубидий — химический элемент из группы щелочных металлов. Его атомный номер 37, а атомная масса примерно равна 85,47. Рубидий имеет серебристо-белый цвет и мягкую консистенцию. Он является одним из наименее плотных металлов, его плотность составляет около 1,5 г/см³.
Рубидий характеризуется низкой температурой плавления. Его точка плавления составляет примерно 39,3°C. Это означает, что при комнатной температуре (около 20°C) рубидий находится в жидком состоянии. Такая низкая температура плавления делает рубидий одним из наиболее подходящих металлов для использования в некоторых специфических технологиях и приборах, где требуется жидкий металл.
Рубидий также обладает низкой температурой кипения. Его точка кипения составляет около 688°C. Это означает, что уже при достаточно низкой температуре рубидий переходит в газообразное состояние. Такие свойства рубидия делают его интересным объектом для исследований в области физики низких температур и газовой динамики.
В таблице Менделеева рубидий располагается после стронция и перед ксеноном. Он назван в честь цвета своих спектральных линий, которые имеют ярко-красный цвет. Рубидий используется в различных областях, включая электронную промышленность, фотодиоды, лазеры, а также в исследованиях биологически активных веществ и магнитных материалов.
Цезий

Цезий (Cs) - химический элемент с атомным номером 55 и символом Cs в периодической системе элементов. Цезий является мягким, серебристо-белым металлом, который легко реагирует с водой, образуя гидроксид цезия. Он является одним из самых активных щелочных металлов.
Цезий имеет наиболее низкую точку плавления среди всех металлов, равную всего лишь 28 градусам Цельсия. Это делает его одним из самых распространенных элементов для использования в калориметрах и термических источниках. В то же время, цезий является одним из наиболее токсичных элементов, поэтому его использование требует особой осторожности.
Цезий также используется в производстве электронных устройств, так как его атомы обладают свойством эмитировать электроны под воздействием света. Также цезий используется в ядерной энергетике, а именно в ядерных реакторах и при создании атомных бомб. Однако из-за его опасности и высокой активности, его использование подвержено строгим правилам и регуляциям.
Изменение температуры плавления металлов от лития до цезия
Температура плавления металлов очень различна и зависит от их структуры и химических свойств. При рассмотрении металлов от лития до цезия можно наблюдать изменение этого параметра.
Литий, находящийся в первой группе периодической таблицы, обладает самой низкой температурой плавления среди всех металлов. Его температура плавления составляет всего около 180 градусов Цельсия. Такая низкая температура обусловлена малым размером атомов лития и слабой межатомной связью.
Вторая группа металлов периодической таблицы включает в себя металлы от бериллия до бария. Температура плавления в этой группе увеличивается по мере увеличения атомного номера. Например, для бериллия, металла с двухатомной кристаллической решеткой, температура плавления составляет около 1287 градусов Цельсия, в то время как для бария, металла с кубической решеткой, она равна примерно 727 градусов Цельсия.
Третья группа металлов периодической таблицы включает в себя скандий, иттрий, лантан, актиний и остальные лантаноиды. Температура плавления металлов в этой группе неоднородна и зависит от их структуры и электронной конфигурации.
Температура плавления металлов от лития до цезия демонстрирует изменение, связанное с химическими и физическими свойствами каждого отдельного металла. Это свидетельствует о важности этих металлов в различных областях науки и техники, где требуется использование разных плавящихся материалов.
Влияние атомной структуры
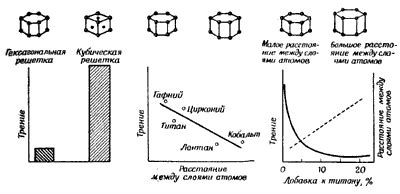
Атомная структура металлов играет важную роль в их температуре плавления. Она определяется расположением атомов и их взаимодействием друг с другом. Влияние атомной структуры на температуру плавления можно объяснить с помощью нескольких ключевых факторов.
Во-первых, атомы металлов могут быть организованы в кристаллической или аморфной структуре. Кристаллическая структура имеет строго определенное расположение атомов, что делает ее более устойчивой и твердой. В аморфной структуре атомы располагаются хаотически, что делает ее менее устойчивой и мягкой. Поэтому кристаллические металлы имеют более высокую температуру плавления, чем аморфные.
Во-вторых, атомы металлов могут образовывать различные типы связей: металлическую, ионную или ковалентную. Связь между атомами определяет их взаимодействие при нагревании. Металлическая связь характеризуется перемещением электронов между атомами, что способствует их подвижности и позволяет металлам иметь высокую температуру плавления. Ионная и ковалентная связи имеют более жесткую структуру и требуют большего количества энергии для разрушения. Поэтому металлы с металлической связью обычно имеют более низкую температуру плавления, чем металлы с ионной или ковалентной связью.
В-третьих, размер и форма атомов также влияют на температуру плавления металлов. Маленькие и компактные атомы имеют более сильные связи и высокую температуру плавления. Например, у металлов из группы переходных элементов атомные радиусы с увеличением заряда ядра уменьшаются, что ведет к повышению температуры плавления. Форма атомов также важна: сферические атомы имеют более компактную структуру, чем атомы с несферической формой, что влияет на их температуру плавления.
Применение в промышленности
Металлы от лития до цезия находят широкое применение в промышленности благодаря своим уникальным свойствам и высокой температуре плавления.
Одно из основных применений этих металлов - производство аккумуляторов. Литий-ионные аккумуляторы, содержащие литий, являются одними из самых эффективных и мощных аккумуляторов на сегодняшний день. Они используются в мобильных устройствах, электромобилях, беспроводных инструментах и других устройствах, где требуется долгая работа без подзарядки.
Кроме того, металлы от лития до цезия также используются в производстве ядерного топлива. Литий и цезий являются важными компонентами в процессе ядерного синтеза и используются для усиления реакции и создания высокой температуры.
Эти металлы также находят применение в космической промышленности. Сплавы на основе металлов от лития до цезия обладают высокой теплопроводностью и низкой плотностью, что делает их идеальными материалами для конструкции космических аппаратов. Они применяются в теплозащитных экранах, двигателях и других компонентах, которые должны выдерживать экстремальные температуры космического пространства.
Также стоит отметить, что эти металлы используются в производстве электроники. Например, металлы от лития до цезия используются для создания полупроводниковых материалов, светодиодов, лазеров и других электронных компонентов.
Вопрос-ответ
Почему температура плавления металлов растет от лития до цезия?
Температура плавления металлов растет от лития до цезия из-за изменения их атомных структур. При переходе от лития к цезию происходит увеличение количества электронов во внешней оболочке. Это приводит к сильному притяжению между атомами, что делает их более устойчивыми и требующими более высоких температур для плавления.
Как изменение массы атомов влияет на температуру плавления металлов?
Изменение массы атомов влияет на температуру плавления металлов путем изменения их атомных структур. Чем больше масса атома, тем более сильным является его взаимодействие с другими атомами. Это приводит к увеличению сил притяжения между атомами, что требует более высоких температур для плавления металла.
Есть ли какая-то зависимость между температурой плавления металлов и их химическими свойствами?
Да, есть зависимость между температурой плавления металлов и их химическими свойствами. Высокая температура плавления может свидетельствовать о высокой устойчивости металла к химическим реакциям и окислению. Некоторые металлы, такие как платина и их химической стойкостью, обладают очень высокими температурами плавления.
Есть ли исключения из общей тенденции роста температуры плавления от лития до цезия?
Да, есть исключения из общей тенденции роста температуры плавления от лития до цезия. Например, жидкий амальгамный сплав натрия и калия имеет меньшую температуру плавления, чем любой из этих элементов по отдельности. Это связано с образованием стабильной сети между атомами, что понижает точку плавления.
Как связана температура плавления металлов с их кристаллической структурой?
Температура плавления металлов связана с их кристаллической структурой. Металлы образуют кристаллическую решетку, в которой атомы или ионы располагаются в определенном порядке. Высокая температура плавления обычно означает, что кристаллическая структура металла требует большой энергии для разрушения и перехода в жидкое состояние.