Двухвалентные металлы представляют собой важный класс химических элементов, обладающих особыми свойствами и широким спектром применения. Они играют ключевую роль в различных отраслях промышленности, науки и технологий. Двухвалентные металлы получают подобными способами, как и другие металлы, но они обладают специфическими химическими и физическими свойствами, которые делают их особенно полезными для различных процессов и приложений.
В список двухвалентных металлов входят такие элементы, как ванадий, хром, железо, марганец, никель и другие. Они характеризуются наличием двух различных степеней окисления, что отражается в их химической формуле и возможности образования соединений с различным количеством электронов. Такое свойство делает их важными катализаторами реакций, промежуточными продуктами при производстве различных веществ, а также основными компонентами многих сплавов и металлических материалов.
Двухвалентные металлы обладают высокой электропроводностью, механической прочностью и химической стабильностью. Они также обладают некоторыми магнитными свойствами и способностью образовывать различные кристаллические структуры. Эти свойства делают их важными компонентами многих электронных устройств, солнечных батарей, автомобильных аккумуляторов, магнитов и других технических изделий.
Кроме того, двухвалентные металлы обладают химической реактивностью, их соединения используются в различных процессах синтеза и каталитических реакциях. Из-за своих физических и химических свойств, двухвалентные металлы играют важную роль в сфере экологии и охране окружающей среды. Например, некоторые из них используются в производстве катализаторов для очистки отработанных газов и воды от вредных примесей и загрязнений.
В данной статье представлен список и основные свойства двухвалентных металлов, а также их применение в различных областях современной науки и технологий.
Двухвалентные металлы: список

Двухвалентные металлы - это класс элементов периодической таблицы, которые имеют две возможные степени окисления. Они способны образовывать соединения с различными элементами и входят в состав многих важных соединений и материалов.
Список двухвалентных металлов включает такие элементы, как:
- Магний (Mg): Магний является лёгким двухвалентным металлом, который используется в различных отраслях, включая производство автомобилей, аэрокосмической промышленности и медицинского оборудования.
- Цинк (Zn): Цинк также является двухвалентным металлом и широко используется в производстве литейных сплавов, оцинкованных изделий, а также в качестве катализаторов в химической промышленности.
- Кадмий (Cd): Кадмий является тяжёлым металлом, который также может образовывать соединения с двумя степенями окисления. Он используется в электронике, аккумуляторах и солнечных панелях.
- Сурьма (Sb): Сурьма также относится к двухвалентным металлам и широко применяется в производстве полупроводников, лекарств и косметических средств.
Важно отметить, что это лишь некоторые представители класса двухвалентных металлов, и в природе существуют и другие элементы с аналогичными свойствами.
Переходные металлы
Переходные металлы — это класс элементов в периодической системе, расположенных между группами 2 и 13. Они отличаются особыми химическими и физическими свойствами, что делает их особенно интересными для исследований.
Одной из главных характеристик переходных металлов является их способность образовывать различные валентности. Большинство переходных металлов могут образовывать соединения с разными степенями окисления, что делает их полезными для реакций окисления-восстановления.
Переходные металлы также обладают высокой термической и электрической проводимостью, что делает их неотъемлемым компонентом многих технологий и промышленных процессов. Их способность образовывать стабильные соединения позволяет им использоваться в катализе и производстве различных материалов.
Список переходных металлов включает такие элементы, как титан (Ti), ванадий (V), хром (Cr), марганец (Mn), железо (Fe), никель (Ni), медь (Cu), цинк (Zn), и др. Каждый из этих элементов имеет свои уникальные свойства и применения.
Причастность к классу переходных металлов делает эти элементы особо важными для различных областей науки и техники. Изучение и использование свойств переходных металлов является ключевым аспектом современной химии и материаловедения.
Алкалий
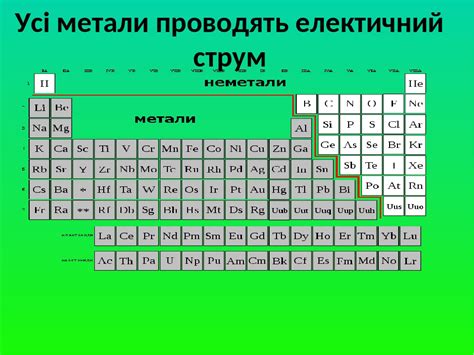
Алкалии - это группа химических элементов, относящихся к двухвалентным металлам. Группа алкалиевых металлов включает такие элементы, как литий, натрий, калий, рубидий, цезий и франций.
Основные характеристики алкалиевых металлов включают низкую плотность, низкую температуру плавления и высокую химическую реактивность. Они также обладают высокой электропроводностью и образуют стабильные и легкорастворимые соединения с другими элементами.
Алкалий металлы широко используются в различных областях, включая производство щелочных батарей, сплавов и стекла. Некоторые алкалии, такие как калий и натрий, необходимы для нормального функционирования организма и являются важными макроэлементами в пище.
Важно отметить, что алкалии имеют очень высокую реактивность и могут быть опасными в обращении. Они реагируют с водой, оксигеном и многими другими веществами, что может привести к возгоранию или взрыву. Поэтому при работе с алкалиями необходимо соблюдать все необходимые меры предосторожности.
В таблице Менделеева алкалии расположены в первой группе и имеют одинарную положительную заряд. Они образуют легко ионизирующиеся ионы, что делает их стабильными и очень реактивными в химических реакциях.
Таким образом, алкалий металлы имеют широкий спектр применений и являются важными элементами в нашей повседневной жизни.
Алкалиноземельные металлы
Алкалиноземельные металлы, также известные как группа 2 или IIА периодической системы химических элементов, представлена шестью элементами: бериллием (Be), магнием (Mg), кальцием (Ca), стронцием (Sr), барием (Ba) и радием (Ra). Эти элементы обладают двухвалентной окислительной способностью, что означает, что они способны образовывать соединения с валентностью +2.
Основные свойства алкалиноземельных металлов заключаются в их химической реактивности и металлических характеристиках. Например, они имеют низкую электроотрицательность, что делает их хорошими веществами-оксидANTами. Эти металлы обладают высокой теплопроводностью и электропроводностью, что позволяет им использоваться в различных промышленных и научных приложениях.
Алкалиноземельные металлы широко распространены в природе и встречаются как в свободном состоянии, так и в виде соединений. Например, бериллий находится в минералах берилл, а магний в магнезитеЕ. Кальций, стронций и барий распространены в земной коре и морских отложениях. Радий, в свою очередь, является радиоактивным элементом и имеет очень короткий период полураспада.
Алкалиноземельные металлы широко используются в различных отраслях промышленности и науки. Например, бериллий используется в производстве ядерных и аэрокосмических материалов, а магний - в производстве сплавов и легких конструкций. Кальций используется в производстве стекла и цемента, стронций - в производстве красок и пиротехнических изделий, а барий - в рентгенологии и производстве стекла.
Получение двухвалентных металлов

Двухвалентные металлы могут быть получены различными способами в зависимости от их характеристик и физических свойств. Одной из методик является использование электролитического способа, при котором вещество растворяется в электролите и затем происходит осаждение металла на электроде. Этот процесс может быть контролируемым с помощью регулирования тока и напряжения.
Другим способом получения двухвалентных металлов является помещение соответствующего вещества в реакционную среду с определенной температурой и давлением. Также может использоваться взаимодействие металла с кислородом или другими реактивами, что приводит к образованию оксидов металла. После этого может происходить процесс восстановления оксида до двухвалентного металла.
Одним из перспективных направлений получения двухвалентных металлов является использование метода газофазного осаждения. При этом используется реакция взаимодействия паров металла с газообразным реагентом. Метод позволяет получать чистые и однородные образцы металлов с высокой степенью чистоты и кристаллической структуры.
Двухвалентные металлы: свойства
Двухвалентные металлы – это элементы химической системы, которые обладают двумя возможными степенями окисления. Свойства этих металлов имеют свои особенности и широко применяются в различных областях.
Одно из основных свойств двухвалентных металлов – высокая реакционная способность. Они легко вступают в химические реакции с другими веществами, что делает их важными компонентами в различных химических процессах. Благодаря этому свойству, двухвалентные металлы широко используются в катализаторах, электродах и других химических процессах.
Еще одним важным свойством двухвалентных металлов является их способность образовывать стойкие соединения с кислородом. Это свойство делает их незаменимыми компонентами в производстве керамики, стекла и других материалов. Более того, некоторые двухвалентные металлы, такие как железо и медь, имеют способность кислородировать, что позволяет им участвовать в окислительно-восстановительных реакциях.
Также двухвалентные металлы обладают хорошими магнитными свойствами. Они являются ферромагнетиками и могут образовывать постоянные магниты. Это делает их важными компонентами в производстве магнитных материалов, таких как магниты, магнитные диски и другие устройства с магнитным полем.
Наконец, двухвалентные металлы обладают высокой электропроводностью. Они являются хорошими проводниками электрического тока и часто используются в электронике и электротехнике. Благодаря высокой электропроводности, двухвалентные металлы могут быть использованы в различных приборах, цепях и электрических устройствах.
Электрохимические свойства

Двухвалентные металлы обладают различными электрохимическими свойствами, которые определяют их способность взаимодействовать с другими веществами в электрохимических реакциях.
Одной из основных характеристик электрохимического поведения металлов является их электропотенциал. Величина электропотенциала показывает, насколько легко металл может отдавать или принимать электроны при участии в электрохимических реакциях. У двухвалентных металлов электропотенциалы могут быть различными и зависят от их химической природы и строения.
Другой важной характеристикой является реакция металла с кислородом. Многие двухвалентные металлы реагируют с кислородом воздуха, образуя оксиды. Эта реакция может быть стабильной и нежелательной для сохранения металла, так как оксиды часто образуют защитные пленки на поверхности металла, предотвращающие дальнейшую коррозию.
Помимо этого, двухвалентные металлы могут участвовать в реакциях окисления-восстановления, при которых они могут менять свою степень окисления. Это позволяет им быть хорошими катализаторами в реакциях электролиза, где происходит превращение одного вещества в другое с помощью электрического тока.
Также двухвалентные металлы могут образовывать различные типы соединений, например, солянокислотные соли или комплексные соединения. Это позволяет им иметь широкий спектр применения в различных областях, включая химическую промышленность, электронику и катализ.
Итак, электрохимические свойства двухвалентных металлов определяют их способность взаимодействовать с другими веществами, образовывать разнообразные соединения и использоваться в различных областях науки и промышленности.
Физические свойства
Двухвалентные металлы обладают рядом характерных физических свойств, которые отличают их от других элементов. Одной из основных характеристик является высокая плотность этих металлов. Это связано с их атомной структурой и способностью образовывать компактные кристаллические решетки.
Другим важным свойством двухвалентных металлов является их степень проводимости электричества. Эти металлы хорошие проводники тока благодаря наличию свободных электронов в своей валентной оболочке. Это позволяет им эффективно передавать электрический заряд и использоваться в различных электроустройствах.
Одной из интересных особенностей двухвалентных металлов является их способность к деформации без разрушения. Это связано с высокой пластичностью, которую они обладают. Они способны подвергаться механическому воздействию без образования трещин и разрывов.
Кроме того, двухвалентные металлы обладают высокой теплопроводностью. Это свойство позволяет им эффективно передавать тепловую энергию и использоваться в процессах теплообмена. Благодаря этой характеристике, они применяются в различных теплотехнических устройствах.
Также стоит отметить, что двухвалентные металлы обладают высокой плотностью электронов в своей валентной оболочке. Это обеспечивает им способность магнетизироваться, что делает их полезными материалами для производства постоянных магнитов и других магнитных устройств.
Вопрос-ответ
Что такое двухвалентные металлы?
Двухвалентные металлы - это металлические элементы, которые имеют два валентных состояния, при которых они могут образовывать соединения. В одном валентном состоянии металл имеет низкую степень окисления, а в другом - высокую.
Какие металлы относятся к двухвалентным?
К двухвалентным металлам относятся такие элементы, как железо, медь, никель, кобальт, марганец и многие другие. Эти металлы могут образовывать соединения с разными степенями окисления в зависимости от условий их окружения.
Каковы свойства двухвалентных металлов?
Свойства двухвалентных металлов варьируются в зависимости от их валентного состояния. В низкоокисленном состоянии они обычно обладают хорошей проводимостью электричества и тепла, высокой пластичностью и прочностью. В высокоокисленном состоянии они могут образовывать стабильные и химически активные соединения.
Какие соединения образуют двухвалентные металлы?
Двухвалентные металлы могут образовывать разнообразные соединения, такие как оксиды, сульфиды, хлориды и другие. В низкоокисленном состоянии, металлы могут образовывать соединения с низкой степенью окисления, например, хлорид железа (FeCl2).
Какие применения имеют двухвалентные металлы?
Двухвалентные металлы находят широкое применение в разных областях. Например, железо используется для производства стали, которая применяется в строительстве и машиностроении. Медь используется в электротехнике и проволочной промышленности. Никель применяется в производстве батареек и монет.
Какие преимущества имеют двухвалентные металлы?
Двухвалентные металлы обладают рядом преимуществ, таких как хорошая проводимость электричества и тепла, высокая прочность и пластичность, а также возможность образования различных химических соединений с разными характеристиками. Это делает их полезными в разных областях промышленности и производства.

