Анодное растворение металла — это процесс, при котором металл под воздействием внешних факторов растворяется в агрессивной среде, превращаясь в ионы. Этот процесс имеет ряд серьезных последствий и может привести к разрушению металлических конструкций, а также к ухудшению их работоспособности.
Причинами анодного растворения металла могут быть различные факторы, такие как наличие оксидов и солей, высокая температура, кислотные или щелочные среды. Особенно подвержены растворению металлы с большой электрохимической активностью, такие как алюминий, железо, цинк и другие.
Механизм анодного растворения металла основан на электрохимической реакции, в которой металл выступает в роли анода, а окружающая среда — в роли катода. При этом на поверхности анода образуются ионы металла, которые растворяются в среде и перемещаются к катоду. Этот процесс сопровождается выделением электрической энергии и может приводить к коррозии металлических поверхностей и деталей.
Последствия анодного растворения металла могут быть разнообразными и в значительной степени зависят от условий процесса. Они могут включать в себя изменение размеров и формы металлических деталей, образование трещин и пузырьков, изменение химического состава материала, а также снижение прочности и надёжности конструкций.
Для предотвращения анодного растворения металла широко применяются различные методы защиты, включая использование противокоррозионных покрытий, анодной защиты и правильного выбора материала. Это позволяет увеличить срок службы и надёжность металлических конструкций, а также снизить вероятность аварийных ситуаций и экономические потери.
Анодное растворение металла
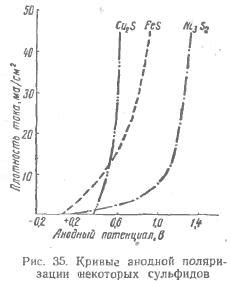
Анодное растворение металла – это процесс, при котором анодный металл растворяется в электролите под воздействием электрического тока. Этот процесс может происходить в различных средах, таких как водные растворы, кислоты, щелочи и другие.
Причинами анодного растворения металла могут быть различные факторы. Одна из основных причин – наличие коррозионной среды, которая способствует активации процесса растворения анода. Также важную роль играет разность потенциалов между анодом и катодом, которая вызывает движение ионов металла от анода к катоду.
Механизм анодного растворения металла включает в себя несколько стадий. Сначала происходит окисление металла, при котором образуются положительно заряженные ионы металла. Затем эти ионы перемещаются через электролит к катоду, где происходит восстановление металла.
Анодное растворение металла имеет свои последствия. Оно может привести к уменьшению массы и размера анодного металла, что может привести к его деформации и потере прочности. Также анодное растворение может вызвать образование пустот, трещин и других дефектов на поверхности металла.
Для предотвращения анодного растворения металла используются различные защитные методы. Один из них – покрытие анода защитным слоем, который предотвращает контакт металла с коррозионной средой. Другой метод – использование анодов из материалов, устойчивых к коррозии, такими как платина, титан и другие.
Процесс анодного растворения
Анодное растворение металлов – это электрохимический процесс, при котором металлическая поверхность анода растворяется в электролите. Он является одним из основных механизмов коррозии металлов.
Процесс анодного растворения начинается с образования оксидной пленки на поверхности металла. При наличии электрического поля, оксидная пленка распадается на ионы и электроны. Ионы металла перемещаются в электролите, а электроны перемещаются по проводящей структуре металла к катоду.
При анодном растворении происходит ускоренное разрушение поверхности металла из-за протекания электролитических процессов. Механизмы анодного растворения могут быть различными в зависимости от металла и условий окружающей среды.
Последствия анодного растворения металла могут быть разрушение конструкций, уменьшение толщины деталей, изменение их формы и размеров. Для предотвращения анодного растворения применяются различные способы защиты, такие как покрытия, антикоррозионные покрытия и применение анодных защитных систем.
Механизм анодного растворения
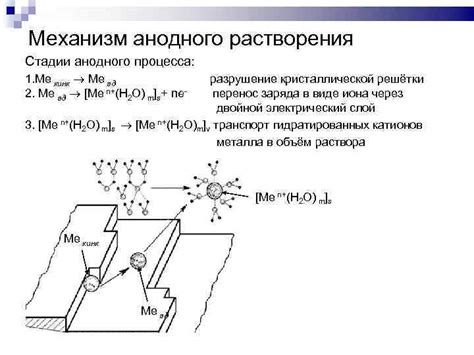
Механизм анодного растворения активных металлов основывается на электрохимических процессах, происходящих на поверхности металла в агрессивной среде. При анодном растворении металла его поверхность под действием окислительного потенциала окисляется и постепенно передается в раствор в виде ионов.
Процесс анодного растворения сложен и состоит из нескольких стадий. Сначала на поверхности металла образуется окислительная пленка, состоящая из окисленных ионов металла. Пленка обладает различной проницаемостью и толщиной в зависимости от металла и условий окружающей среды.
Далее, под воздействием электрического поля, ионы металла с поверхности постепенно диффундируют в раствор и переносятся к аноду, где они участвуют в реакциях редокс. Таким образом, металл постепенно теряет свою массу и создается раствор, содержащий ионы металла.
В процессе анодного растворения металла важную роль играет концентрация ионообразующих примесей в растворе, pH среды, температура, сила электрического поля и другие факторы. Эти параметры могут влиять на скорость анодного растворения и приводить к изменению свойств металла, например, его механической прочности или долговечности.
Причины анодного растворения
Анодное растворение металла – это процесс, при котором металлический анод растворяется в электролите. В результате анодного растворения металл теряет свою массу и объем, что может привести к разрушению и повреждению конструкций, на которых он используется.
Основной причиной анодного растворения металла является процесс коррозии – химическое взаимодействие металла с окружающей средой. При наличии электролита (например, влажности или раствора) и наличии электрической проводимости, металл может выступать в роли анода – положительно заряженного электрода.
В результате анодного растворения металла происходит перенос металлических ионов из анода в электролит. Это связано с электрохимическими процессами на поверхности металла – окислительно-восстановительными реакциями. Металлические ионы могут быть растворены в электролите или они могут выпадать на другую поверхность в виде нерастворимых соединений.
Один из основных факторов, влияющих на анодное растворение металла, это потенциал окисления. Для каждого металла существует определенный потенциал окисления, при котором начинается процесс анодного растворения. Если этот потенциал достигается, то металл начинает активно растворяться в электролите.
Важным фактором, влияющим на анодное растворение металла, является pH-значение электролита. Некоторые металлы могут быть особенно подвержены анодному растворению при определенных значениях pH. Кроме того, влияние на анодное растворение металла оказывают и другие факторы, такие как температура, концентрация электролита, наличие примесей и т. д.
Последствия анодного растворения
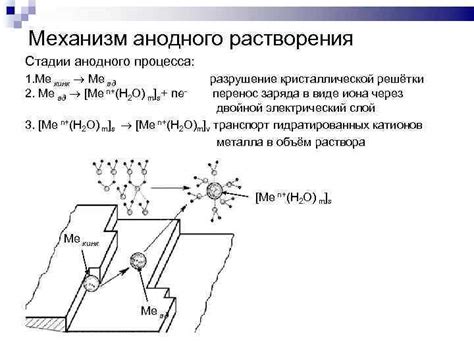
Анодное растворение металла является процессом, который может привести к различным негативным последствиям. Одним из них является уменьшение толщины металлического изделия в результате потери материала вследствие растворения анода. Это может привести к ослаблению структуры и повышению вероятности разрушения изделия.
Еще одним последствием анодного растворения является появление коррозии металла. При воздействии на металл окружающей среды и электролита, происходит запуск и протекание различных химических реакций, которые под влиянием анодного растворения могут привести к образованию коррозионных продуктов и повреждению поверхности металла.
Также, анодное растворение может приводить к утрате функциональности изделия. Например, в электрохимических аккумуляторах анодный материал является источником электронов, необходимых для работы батареи. Если анод растворяется, то происходит потеря электродного материала и, следовательно, снижение производительности аккумулятора.
Кроме того, анодное растворение может привести к необратимым изменениям в химическом составе и структуре металла. Это может негативно сказаться на его механических свойствах и вызвать деформации или разрушение изделия. Поэтому контроль и предотвращение анодного растворения является важной задачей при проектировании и эксплуатации металлических конструкций и изделий.
Вопрос-ответ
Почему металлы подвержены анодному растворению?
Металлы могут подвергаться анодному растворению из-за разности потенциалов между металлом и окружающей средой. Это происходит из-за электрохимического процесса, при котором электроны переносятся с поверхности металла на ионы окружающего раствора, что приводит к образованию раствора металла.
Какие факторы влияют на скорость анодного растворения металла?
Скорость анодного растворения металла зависит от нескольких факторов, включая характеристики металла (например, его электрохимический потенциал) и условия окружающей среды (такие как температура, содержание кислорода или других электроактивных веществ). Также важным фактором является поверхностная область металла, доступная растворению.
Какие последствия может иметь анодное растворение металла?
Анодное растворение металла может привести к различным негативным последствиям. В некоторых случаях это может привести к коррозии и разрушению металлических конструкций, что может быть опасно, особенно если речь идет о конструкциях, которые находятся в критическом состоянии (например, авиационные или судовые конструкции). Кроме того, анодное растворение может приводить к потере материала и ухудшению эффективности работы металлических изделий.
Как можно предотвратить анодное растворение металла?
Существует несколько способов предотвращения анодного растворения металла. Один из них - использование защитных покрытий на поверхности металла, таких как краски или пленки, которые предотвращают контакт металлической поверхности с окружающей средой. Другой способ - использование анодной защиты, при которой на металлическую поверхность наносятся специальные аноды, которые контролируют поток электронов и предотвращают растворение металла.
