Внешний уровень электронной оболочки атома металла определяет его химические свойства и реактивность. В учебниках химии часто утверждается, что у атомов металлов внешним уровнем является s- или p-подуровень. Однако, следует иметь в виду, что не все металлы имеют одинаковое количество электронов на внешнем уровне.
На самом деле, количество электронов на внешнем уровне у атомов металлов может варьироваться. Например, у группы щелочных металлов количество электронов на внешнем уровне составляет 1, в то время как у группы щёлочноземельных металлов – 2. Другие металлы могут иметь иные значения для количества электронов на внешнем уровне.
Важно отметить, что количество электронов на внешнем уровне влияет на химическую активность металлов. Так, атомы металлов с одним электроном на внешнем уровне имеют большую склонность к донорству этого электрона, образуя положительный ион. В свою очередь, металлы с двумя электронами на внешнем уровне образуют два положительных иона, что сказывается на их реакционной способности.
Сколько электронов на внешнем уровне у атомов металлов?

У атомов металлов количество электронов на внешнем (валентном) уровне может варьироваться в зависимости от их положения в периодической таблице элементов. Валентный уровень - это наиболее энергетически удаленный уровень электронной оболочки атома, на котором происходят химические реакции и образуются химические связи.
У большинства металлов на внешнем уровне находится от 1 до 3 электронов. Например, у атомов щелочных металлов (литий, натрий, калий и др.) на внешнем уровне находится один электрон. У атомов щелочноземельных металлов (магний, кальций, барий и др.) на внешнем уровне находятся два электрона. А у атомов металлов переходных элементов количество электронов на внешнем уровне может быть от 1 до 3 или более, в зависимости от конкретного элемента.
Валентность металлов определяет их химическую активность и способность образовывать ионы и соединения с другими элементами. Металлы с одним электроном на внешнем уровне (валентность 1) обладают большей активностью и склонностью к образованию однозарядных ионов, чем металлы с двумя электронами на внешнем уровне (валентность 2) и металлы с тремя электронами на внешнем уровне (валентность 3).
В связи с этим, металлы разных групп периодической таблицы обладают различной реакционной способностью и образуют разнообразные химические соединения. Например, щелочные металлы проявляют высокую реакционную способность и легко образуют ионы с однозарядным положительным зарядом, а металлы переходных элементов образуют ионы разной валентности и обладают большим разнообразием химических свойств.
Количество электронов на внешнем уровне в атомах металлов - основная характеристика
Количество электронов на внешнем уровне является одной из основных характеристик атомов металлов. В каждом атоме металла, на внешнем энергетическом уровне находится определенное число электронов, которое определяет химические свойства и способность атома образовывать соединения.
Металлы отличаются от других элементов тем, что у них на внешнем уровне находится всего несколько электронов. В результате этого, атомы металлов имеют свободные или подвижные электроны, которые могут легко передвигаться по сети кристаллической решетки металла. Именно это делает металлы хорошими проводниками электричества и тепла.
Количество электронов на внешнем уровне металлов может варьироваться от одного до трех. У металлов из группы щелочных металлов (например, натрия и калия) на внешнем уровне всего один электрон, а у металлов из группы щелочноземельных металлов (например, магния и кальция) - два электрона. Металлы из группы переходных металлов (такие как железо и медь) имеют от одного до трех электронов на внешнем уровне, в зависимости от своего положения в периодической системе.
Общая тенденция заключается в том, что чем меньше электронов на внешнем уровне у атома металла, тем он более активен в химических реакциях и образовании соединений. Это связано с тем, что атомы металлов стремятся передать свои внешние электроны другим атомам, чтобы достичь более устойчивой конфигурации энергетических уровней.
Таким образом, количество электронов на внешнем уровне - важный показатель, который определяет химические свойства и реактивность атомов металлов, а также их способность образовывать соединения с другими элементами.
Атомы металлов на внешнем уровне имеют малое количество электронов
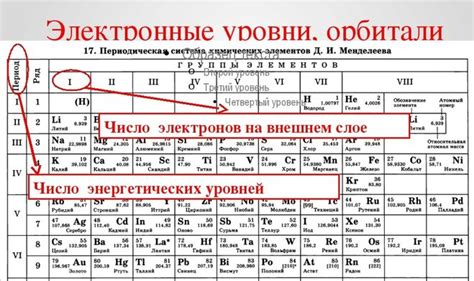
Атомы металлов, находящиеся в периодической системе элементов, обладают уникальными свойствами, одним из которых является малое количество электронов на их внешнем энергетическом уровне. В отличие от неметаллов, у которых валентная оболочка содержит много электронов, атомы металлов имеют всего несколько электронов на своем внешнем энергетическом уровне.
Это свойство делает электроны на внешнем периферическом уровне у атомов металлов слабо удерживаемыми ядром и, следовательно, свободными для участия в химических реакциях. Именно эти свободные электроны обеспечивают металлы их уникальными физическими и химическими свойствами, такими как высокая электропроводность и теплопроводность.
Малое количество электронов на внешнем уровне у атомов металлов позволяет им образовывать ионы положительного заряда. В результате этого, атомы металлов способны образовывать соли и соединения с неметаллами, передавая свои электроны и образуя ионы с положительным зарядом.
Однако, стоит иметь в виду, что количество электронов на внешнем уровне у атомов металлов может варьироваться в зависимости от их положения в периодической системе. Некоторые металлы, например щелочные металлы, имеют всего один электрон на своем внешнем энергетическом уровне, в то время как другие металлы могут иметь до нескольких электронов на внешней оболочке.
Какие суждения верны?
Начнем с того, что у атомов металлов на внешнем уровне электроны стремятся к образованию ионов с положительным зарядом, чтобы достичь стабильной электронной конфигурации. Как следствие, внешний уровень электронов у атомов металлов обычно состоит из одного, двух или трех электронов.
Следующее верное суждение - у металлов, находящихся в левой части периодической системы, на внешнем уровне обычно находится один или два электрона. Это связано с тем, что атомы металлов стремятся отдать эти электроны и образовать положительные ионы.
Третье суждение - у металлов в правой части периодической системы на внешнем уровне обычно находятся три электрона. Это связано с тем, что атомы металлов в правой части периодической системы стремятся принять три электрона и образовать отрицательные ионы.
Однако стоит отметить, что эти суждения являются общими и могут иметь исключения. Например, для некоторых атомов металлов могут быть характерны более сложные электронные конфигурации на внешнем уровне.
Атомы металлов стремятся отдать электроны на внешнем уровне

Электроны на внешнем энергетическом уровне, также известном как валентный уровень, играют ключевую роль в химических свойствах атомов металлов. Обладая относительно малой привлекательной силой к ядру, эти электроны легко отделяются и могут быть переданы другим атомам. Поэтому атомы металлов обычно стремятся избавиться от электронов на своем внешнем уровне, чтобы достичь более стабильного состояния.
Отдача электронов на внешнем уровне позволяет атомам металлов образовывать ионный связи с атомами неметаллов. Металлы обладают способностью образовывать катионы — положительно заряженные ионы, которые образуются после потери одного или нескольких электронов. Это делает металлы хорошими проводниками электричества и тепла, так как перемещение электронов внутри металлической решетки позволяет легко передавать энергию.
Стоит отметить, что количество электронов на внешнем уровне у атомов металлов может варьироваться в зависимости от их положения в периодической системе. Некоторые металлы имеют только один электрон на внешнем уровне, как, например, литий и натрий, в то время как другие обладают двумя или более электронами в валентной оболочке.
В целом, отдача электронов на внешнем уровне у атомов металлов является следствием их стремления к достижению более устойчивого электронного конфигурации. Это делает атомы металлов активными веществами, способными участвовать в химических реакциях и образовывать соединения с другими элементами.
Вопрос-ответ
Сколько электронов на внешнем уровне у атомов металлов?
У атомов металлов на внешнем уровне обычно находится от 1 до 3 электронов.
Какие суждения верны относительно количества электронов на внешнем уровне у атомов металлов?
Сказать, что у всех атомов металлов одинаковое количество электронов на внешнем уровне неверно. У металлов количество электронов на внешнем уровне может варьироваться от 1 до 3.
Правда ли, что у атомов металлов всегда по 2 электрона на внешнем уровне?
Нет, это неправда. У атомов металлов на внешнем уровне может быть от 1 до 3 электронов. Таким образом, количество электронов на внешнем уровне у атомов металлов может быть разным.
Какое количество электронов на внешнем уровне у атомов металлов?
У атомов металлов на внешнем уровне может находиться 1, 2 или 3 электрона.
Могут ли у атомов металлов быть по 3 электрона на внешнем уровне?
Да, у атомов металлов может быть на внешнем уровне 3 электрона.
Сколько электронов обычно на внешнем уровне у атомов металлов?
Обычно у атомов металлов на внешнем уровне находится 1 или 2 электрона.

